
Wetenschap
Berekening van het aantal mol ammoniumionen in carbonaatverbindingen
1. Identificeer de verbinding:
U vraagt naar het aantal ammoniumionen (NH₄⁺) in een carbonaatmonster. Omdat carbonaten het CO₃²⁻-ion bevatten, moeten we bedenken om welke ammoniumverbinding het gaat. Laten we aannemen dat u ammoniumcarbonaat ((NH₄)₂CO₃) bedoelt , wat een veel voorkomende verbinding is.
2. Bepaal de molaire massa van ammoniumcarbonaat:
* Molaire massa van (NH₄)₂CO₃ =(2 * 14,01 g/mol (N)) + (8 * 1,01 g/mol (H)) + (12,01 g/mol (C)) + (3 * 16,00 g/mol (O))
* Molaire massa van (NH₄)₂CO₃ =96,09 g/mol
3. Bereken het aantal mol ammoniumcarbonaat:
* Mol (NH₄)₂CO₃ =massa / molaire massa
* Mol (NH₄)₂CO₃ =8,718 g / 96,09 g/mol
* Mol (NH₄)₂CO₃ ≈ 0,0907 mol
4. Bepaal de molverhouding van ammoniumionen tot ammoniumcarbonaat:
* In één formule-eenheid van (NH₄)₂CO₃ zijn er twee ammoniumionen (NH₄⁺).
* Daarom is de molverhouding 2:1.
5. Bereken het aantal mol ammoniumionen:
* Mol NH₄⁺ =(mol (NH₄)₂CO₃) * (2 mol NH₄⁺ / 1 mol (NH₄)₂CO₃)
* Mol NH₄⁺ =0,0907 mol * 2
* Mol NH₄⁺ ≈ 0,1814 mol
Daarom zijn er ongeveer 0,1814 mol ammoniumionen in 8,718 g ammoniumcarbonaat.
 Welke belangrijke eigenschappen heeft Breccia dat het een nuttige rots maakt?
Welke belangrijke eigenschappen heeft Breccia dat het een nuttige rots maakt?  Dodental stijgt terwijl tondeldroge omstandigheden dodelijke branden in Californië voeden
Dodental stijgt terwijl tondeldroge omstandigheden dodelijke branden in Californië voeden Wat is een goede definitie van de natuurlijke omgeving?
Wat is een goede definitie van de natuurlijke omgeving?  NASA-NOAA-satelliet volgt overblijfselen van tropische storm Blakes die zich verspreiden
NASA-NOAA-satelliet volgt overblijfselen van tropische storm Blakes die zich verspreiden Uitdunnen van bossen, voorgeschreven vuur vóór droogte verminderde boomverlies
Uitdunnen van bossen, voorgeschreven vuur vóór droogte verminderde boomverlies
Hoofdlijnen
- Komt de bio -synthese van ribosomale subeenheden voor in kern?
- Wat maakt een mens meer dan een dier?
- Wie zijn de drie mannen die de celtheorie hebben ontwikkeld?
- Als we nu veel van dit kwallen GLO -eiwit willen produceren, wat hebben dan na het eerste succesvolle klonen?
- Waarom hebben sommige organellen dubbel membraan?
- Wat wordt er geproduceerd wanneer suiker in een dierencel wordt verteerd?
- Wat zijn de functies van de basis- en armmicroscoop?
- Wat gebruiken witte bloedcellen om bacteriën te overspoelen en te vernietigen die de glycoproteïnen herkennen als niet zelf?
- CG in genomen begrijpen:CpG-dinucleotiden uitgelegd
- Veranderingen in de chiraliteit van moleculen in realtime observeren
- Smeltglazen van niet-smeltbare verbindingen
- Video:Surfside condo instorting en de wetenschap van beton

- Onderzoekers kijken in de databank van waterclusters, treinnetwerk om energielandschappen te voorspellen

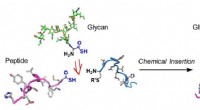
- Een winnende combinatie voor glycoproteïnesynthese
 Goedkoop membraan reinigt lichte en zware oliën in één stap
Goedkoop membraan reinigt lichte en zware oliën in één stap Onderzoekssamenwerking werkt in de richting van tijdige aanpassing aan kustoverstromingen
Onderzoekssamenwerking werkt in de richting van tijdige aanpassing aan kustoverstromingen Hoe sociale media de passies van mensen aanwakkeren - en extremistische verdeeldheid zaaien
Hoe sociale media de passies van mensen aanwakkeren - en extremistische verdeeldheid zaaien Wetenschappers bereiken arylering van C-H-bindingen in milde omstandigheden
Wetenschappers bereiken arylering van C-H-bindingen in milde omstandigheden Welke brandstof wordt gebruikt in kerncentrales?
Welke brandstof wordt gebruikt in kerncentrales?  Samengestelde organische mobiliserende middelen verbeteren de accumulatie van cadmium in sorghum
Samengestelde organische mobiliserende middelen verbeteren de accumulatie van cadmium in sorghum Hoe pooloplossingen kunnen worden versterkt in het wegvervoer
Hoe pooloplossingen kunnen worden versterkt in het wegvervoer  In een atoom de kernenergie in gehouden?
In een atoom de kernenergie in gehouden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

