
Wetenschap
Aluminium- en zinknitraatreactie:het chemische proces begrijpen
Aluminium is reactiever dan zink. Dit betekent dat aluminium zink uit zijn oplossing zal verdringen.
De reactie:
De reactie is een enkele verplaatsingsreactie:
* 2Al(s) + 3Zn(NO₃)₂(aq) → 2Al(NO₃)₃(aq) + 3Zn(s)
Uitleg:
* Aluminium (Al) reageert met zinknitraat (Zn(NO₃)₂) en vormt aluminiumnitraat (Al(NO₃)₃) en vast zink (Zn).
* De aluminiumatomen zullen elektronen verliezen en aluminiumionen worden (Al³⁺), die zich vervolgens zullen combineren met nitraationen (NO₃⁻) om aluminiumnitraat te vormen.
* De zinkionen (Zn²⁺) zullen elektronen verkrijgen en zinkatomen worden, die als vast zink uit de oplossing zullen neerslaan.
Opmerkingen:
* Je ziet een grijsachtig witte vaste stof (zink) ontstaan op het oppervlak van het aluminium.
* De oplossing wordt kleurloos naarmate het zinknitraat wordt verbruikt.
* Het aluminium kan putjes krijgen als het wordt geoxideerd.
Belangrijke opmerking: De reactie zal langzaam verlopen bij kamertemperatuur. Het kan worden versneld door de oplossing te verwarmen of door het oppervlak van het aluminium te vergroten.
 2 bevingen in de buurt van Grieks eiland binnen 7 minuten
2 bevingen in de buurt van Grieks eiland binnen 7 minuten Bevat de toendra naaldbos of bladverliezend bos?
Bevat de toendra naaldbos of bladverliezend bos?  Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan
Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan Baanbrekende fossiele voetafdrukken opgegraven in Kenia onthullen belangrijke inzichten in het gedrag van vroege mensachtigen
Baanbrekende fossiele voetafdrukken opgegraven in Kenia onthullen belangrijke inzichten in het gedrag van vroege mensachtigen  Sommige Amazone-regenwoudgebieden zijn beter bestand tegen klimaatverandering dan eerder werd gedacht
Sommige Amazone-regenwoudgebieden zijn beter bestand tegen klimaatverandering dan eerder werd gedacht
Hoofdlijnen
- Wat voor soort bacteriën was Anabaena?
- Onderzoekers volgen hoe sporen uit de slapende toestand ontsnappen
- Wat betekent biosfeer volgens de wetenschap?
- Waarom carnivoren spanten voedsel verteren?
- Iteracties tussen biotische en abiotische factoren?
- Welke klier heeft een medulla afgeleid van ectoderm en cortex mesoderm?
- Wat voeden schimmels?
- Welke van deze orgelsystemen vereist het minst het zenuwstelsel om te functioneren?
- Bevat de kern genen voor overerving?
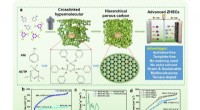
- Meervoudig gedoteerde hiërarchische poreuze koolstoffen voor superieure opslag van zinkionen
- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

- Hoe moleculaire zeven te activeren:een praktische gids voor chemici

- Een potentieel goedkope, efficiënt en milieuvriendelijk systeem voor het zuiveren van aardgas

- De regels overtreden:zware chemische elementen veranderen de theorie van de kwantummechanica

 SpaceX klaar voor vrachtlancering op donderdag naar ruimtestation
SpaceX klaar voor vrachtlancering op donderdag naar ruimtestation Waarom ontwikkelt zich een dipool in molecuul?
Waarom ontwikkelt zich een dipool in molecuul?  Hoe oplosbaarheid te berekenen op basis van KSP
Hoe oplosbaarheid te berekenen op basis van KSP  Hoe krijgen echinoderms hun energie?
Hoe krijgen echinoderms hun energie?  Onderzoek toont aan dat walvissen, al een bedreigde diersoort, kan een vage toekomst tegemoet gaan
Onderzoek toont aan dat walvissen, al een bedreigde diersoort, kan een vage toekomst tegemoet gaan Wat is methacrylzuur?
Wat is methacrylzuur?  Waarom worden planeten genoemd wat ze hebben genoemd?
Waarom worden planeten genoemd wat ze hebben genoemd?  De hoogte- en dieptepunten van de opiumhandel in zuidelijk Afrika
De hoogte- en dieptepunten van de opiumhandel in zuidelijk Afrika
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

