
Wetenschap
Lachgas (N₂O) Intermoleculaire krachten:meer dan dispersie
Dit is waarom:
* Moleculaire structuur: Lachgas heeft een lineaire structuur met het zuurstofatoom aan het ene uiteinde en de stikstofatomen aan het andere uiteinde. Het elektronegativiteitsverschil tussen stikstof en zuurstof creëert een polaire binding , resulterend in een permanent dipoolmoment voor het molecuul.
* Dipool-dipoolinteracties: Door het permanente dipoolmoment kunnen N₂O-moleculen met elkaar interageren via dipool-dipoolkrachten, die sterker zijn dan dispersiekrachten.
* Verspreidingskrachten: Hoewel dipool-dipoolkrachten de dominante intermoleculaire krachten zijn, zijn er ook dispersiekrachten aanwezig in N₂O. Deze krachten komen voort uit tijdelijke fluctuaties in de elektronenverdeling binnen het molecuul.
Samenvattend ervaart distikstofoxide zowel dipool-dipoolinteracties als dispersiekrachten, waarbij dipool-dipoolkrachten de grootste bijdrage leveren aan de algehele intermoleculaire interacties.
 Hoeveel mol ammoniumionen zijn er in 6,965 g carbonaat?
Hoeveel mol ammoniumionen zijn er in 6,965 g carbonaat?  Wat is het verschil tussen secundaire en primaire verontreinigende stoffen?
Wat is het verschil tussen secundaire en primaire verontreinigende stoffen?  Welke natuurlijk voorkomende stof is de beste geleider van elektriciteit?
Welke natuurlijk voorkomende stof is de beste geleider van elektriciteit?  Kan waterstofperoxide door een celmembraan passeren?
Kan waterstofperoxide door een celmembraan passeren?  Bij alfaverval kunnen het ouderelement en de dochter verschillende isotopen van hetzelfde zijn, maar bij bèta zijn ze altijd hetzelfde?
Bij alfaverval kunnen het ouderelement en de dochter verschillende isotopen van hetzelfde zijn, maar bij bèta zijn ze altijd hetzelfde?
 Trump versoepelt de Amerikaanse methaanregels, aangezien Colorado zegt dat staten werken
Trump versoepelt de Amerikaanse methaanregels, aangezien Colorado zegt dat staten werken Slim irrigatiemodel voorspelt regenval om water te besparen
Slim irrigatiemodel voorspelt regenval om water te besparen Studie vindt verminderde voedingsactiviteit van bodemdetritivoren onder warmere en drogere omstandigheden
Studie vindt verminderde voedingsactiviteit van bodemdetritivoren onder warmere en drogere omstandigheden Brazilië verliest een miljoen voetbalvelden aan bos
Brazilië verliest een miljoen voetbalvelden aan bos Kilauea-vulkaan claimt meer dan twee dozijn huizen op Hawaï
Kilauea-vulkaan claimt meer dan twee dozijn huizen op Hawaï
Hoofdlijnen
- Wie is de wetenschapper die zijn primitieve microscoop in 1665 gebruikte om plantmaterialen te observeren, hebben een cellulaire structuur?
- Welke pH zou enzym het meest effectief zijn?
- Wat is fotosytem I en II?
- Een voorbeeld van een biologische universele gebeurtenis die zich op relatief tegelijkertijd in alle samenlevingen voordoet, wordt wat genoemd?
- Wat creëerde de eerste levende micro -organismen op aarde?
- Wat is een aanpassing van de eiercel?
- Dieetbeperking en levensduur bij mannelijke en hermafrodiete wormen
- Wat is genbewerking en hoe kan dit onze toekomst vormgeven?
- Wat is een heterozygoot paar?
- Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van mol per liter

- Goedkoop, schaalbare watersplitsing voedt de toekomstige waterstofeconomie

- Nieuwe methode gebruikt kunstmatige intelligentie om levende cellen te bestuderen
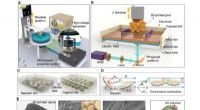
- 3D-printen elektrisch ondersteund, op parelmoer geïnspireerde structuren met zelfgevoelige mogelijkheden
- Wetenschappers hebben ontdekt hoe bloedwormen hun unieke koperen tanden maken

 Waar genen voor een bepaalde eigenschap zijn gevestigd?
Waar genen voor een bepaalde eigenschap zijn gevestigd?  Wat een hoop afval:uit nieuw onderzoek blijkt dat het Britse zwerfvuil wordt gedomineerd door plastic en drankverpakkingen
Wat een hoop afval:uit nieuw onderzoek blijkt dat het Britse zwerfvuil wordt gedomineerd door plastic en drankverpakkingen  Veranderingen in niet-extreme neerslag kunnen minder subtiele gevolgen hebben
Veranderingen in niet-extreme neerslag kunnen minder subtiele gevolgen hebben Leef snel, sterf jong:signaaldetectietheorie bijwerken
Leef snel, sterf jong:signaaldetectietheorie bijwerken Dodelijke orkaan Dorian parkeert zich boven de Bahama's
Dodelijke orkaan Dorian parkeert zich boven de Bahama's DOT- en kruisdiagrammen van de vorming ammoniumionen?
DOT- en kruisdiagrammen van de vorming ammoniumionen?  Het aanpassen van de verwerkingstemperatuur resulteert in betere hydrogels voor biomedische toepassingen
Het aanpassen van de verwerkingstemperatuur resulteert in betere hydrogels voor biomedische toepassingen Hoeveel peroxisomen zijn aanwezig per cel?
Hoeveel peroxisomen zijn aanwezig per cel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

