
Wetenschap
Sigma-obligaties in CH₂Cl₂:een gedetailleerde uitleg
Zo bepaal je het aantal sigmabindingen in CH₂Cl₂ (dichloormethaan):
Sigma-obligaties begrijpen
* Sigma-obligaties (σ-obligaties) zijn het sterkste type covalente binding. Ze worden gevormd door de directe overlap van atomaire orbitalen langs de internucleaire as.
* Enkele obligaties zijn altijd sigma-obligaties.
Het molecuul analyseren
1. Centrale koolstof: Het koolstofatoom in CH₂Cl₂ vormt vier afzonderlijke bindingen:
* Twee bindingen met waterstofatomen (C-H)
* Twee bindingen aan chlooratomen (C-Cl)
2. Waterstof en chloor: Elk waterstof- en chlooratoom vormt één enkele binding (H-C en Cl-C).
De Sigma-obligaties tellen
Daarom zijn er in totaal 4 sigma-obligaties in CH₂Cl₂.
 Cement versus beton:hun verschillen, en kansen voor duurzaamheid
Cement versus beton:hun verschillen, en kansen voor duurzaamheid Wat is de theoretische opbrengst als 50 grammen koper mogen reageren met overtollige chloor 101.6Grammen gevormd?
Wat is de theoretische opbrengst als 50 grammen koper mogen reageren met overtollige chloor 101.6Grammen gevormd?  Wat zou je moeten doen om te bewijzen dat massa behouden blijft tijdens verbrandingsreacties?
Wat zou je moeten doen om te bewijzen dat massa behouden blijft tijdens verbrandingsreacties?  Wetenschappers stemmen het systeem af om syngas te maken uit CO2
Wetenschappers stemmen het systeem af om syngas te maken uit CO2 Wordt Jabir Ibn Hayyan beschouwd als de vader van de chemie?
Wordt Jabir Ibn Hayyan beschouwd als de vader van de chemie?
Hoofdlijnen
- Welk molecuul wordt gevonden in DNA maar geen RNA?
- Hoe regelt een cel het herstel van zijn beschadigde DNA?
- De aanwezigheid van welke organel geeft aan dat eukaryotische cellen zijn geëvolueerd uit prokaryotische cellen?
- Welke drie functies in meercellige organismen bereiken mitose en celdeling?
- Fungeren als opslagzakken in de cel?
- Hoe worden wetenschappelijke schaar genoemd?
- Uit onderzoek blijkt dat het microbioom dynamisch verandert en belangrijke gastheerrelevante functies begunstigt
- Wat zijn de bouwstenen (of basismonomeren) van DNA?
- Wat zijn de soorten polutie?
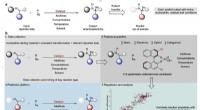
- Een nieuwe methode om zwavel in complexe moleculen te installeren

- De kans op succes in de synthetische chemie vergroten
- Gebruik van nabij-infrarood licht om een oor in het lichaam in 3D te printen

- Nieuwe generatie materiaal verwijdert jodium uit water

- Technieken voor het verlagen van het suikergehalte in zuivelproducten zijn veelbelovend

 Wat is de oxidatie van xeof4?
Wat is de oxidatie van xeof4?  Onderzoekers identificeren een metaal dat bestand is tegen ultrahoge temperatuur en druk
Onderzoekers identificeren een metaal dat bestand is tegen ultrahoge temperatuur en druk De terugkeer van de Blob kan de gevolgen van de klimaatverandering voor de visserij in het noordoosten van de Stille Oceaan versterken
De terugkeer van de Blob kan de gevolgen van de klimaatverandering voor de visserij in het noordoosten van de Stille Oceaan versterken Hoeveel mol NaCl worden gevormd uit de reactie tussen 1,4 HCl en 2,8 NaOH?
Hoeveel mol NaCl worden gevormd uit de reactie tussen 1,4 HCl en 2,8 NaOH?  Heeft geleidbaarheid invloed op de diffusiesnelheid?
Heeft geleidbaarheid invloed op de diffusiesnelheid?  Wat beschrijft het beste hoe wetenschappers het Hunan -gen hebben gevonden dat insuline maakt?
Wat beschrijft het beste hoe wetenschappers het Hunan -gen hebben gevonden dat insuline maakt?  Studie vindt verband tussen financiële angst van leraren en werkprestaties
Studie vindt verband tussen financiële angst van leraren en werkprestaties We moeten af van koolstof in de atmosfeer, niet alleen de uitstoot verminderen
We moeten af van koolstof in de atmosfeer, niet alleen de uitstoot verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

