
Wetenschap
Wat is de oxidatie van xeof4?
Oxidatietoestanden begrijpen
* oxidatietoestand Is de hypothetische lading die een atoom zou hebben als al zijn obligaties 100% ionisch waren.
* fluor (f) Heeft altijd een oxidatietoestand van -1 in zijn verbindingen.
* zuurstof (O) heeft meestal een oxidatietoestand van -2, behalve in peroxiden (waar het -1 is).
De regels toepassen
1. Oxidatietoestanden toewijzen aan F en O:
* Er zijn vier fluoratomen (4 x -1 =-4)
* Er is één zuurstofatoom (-2)
2. Laat de oxidatietoestand van Xe 'x' zijn.
3. Stel een vergelijking in:
* x + (-4) + (-2) =0 (de som van oxidatietoestanden in een neutraal molecuul is nul)
4. Los op voor 'x':
* x - 6 =0
* x =+6
Daarom is de oxidatietoestand van XE in Xeof₄ +6.
 Hoe zijn palmbomen nuttig in de woestijn?
Hoe zijn palmbomen nuttig in de woestijn?  Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen
Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen  NASA-infraroodgegevens laten zien dat Cristina sterker wordt
NASA-infraroodgegevens laten zien dat Cristina sterker wordt We gaan naar Miss Our Temperature Goals: Here's What it means For You
We gaan naar Miss Our Temperature Goals: Here's What it means For You  Onderzoek maakt het mogelijk om slimmer te plannen, veerkrachtigere steden
Onderzoek maakt het mogelijk om slimmer te plannen, veerkrachtigere steden
Hoofdlijnen
- Noem de modus van voeding in ronde worm en Plasmodium?
- Fatale hechting:hoe pathogene bacteriën zich aan het slijmvlies hechten en afschilfering voorkomen
- Wat is het belangrijkste product van fotosynthese dat in planten is opgeslagen?
- Waarom is het zo moeilijk voor mensen om een baby te krijgen?
- Wetenschappers ontgrendelen de code om betere erwten te kweken
- Honden in de winter beschermen tegen extreme kou, ijs, zout en deicers
- Ontdekking van oud glasvezelfossiel uit Glasgow onthult nieuwe soorten
- Welke structuur verwijst naar de draaiende spiraalvormige vorm gevormd door sequentie en eigenschappen van aminozuren?
- Welk idee van gebaseerd op fossielen en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetische veranderingen worden geërfd door latere generatie?
- Een nieuw mechanisme in celdeling ontdekken
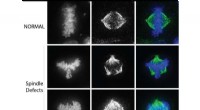
- Het maken van mazen met behulp van het Turings wiskundig model resulteert in efficiënte waterfilters

- Versterking van passieve bemonstering van niet-polaire chemicaliën

- Selectief kooldioxide omzetten in methaan of ethaan

- Organotinvergiftiging kan zwaarlijvigheid veroorzaken, medici zeggen:
 Zijn zeer kleine eenvoudige cellen zonder kern?
Zijn zeer kleine eenvoudige cellen zonder kern?  Geometrisch volume aan kinderen leren
Geometrisch volume aan kinderen leren Nieuwe beeldvormingstechniek helpt bij het oplossen van nanodomeinen, chemische samenstelling in celmembranen
Nieuwe beeldvormingstechniek helpt bij het oplossen van nanodomeinen, chemische samenstelling in celmembranen Qubits in achteruit gezet
Qubits in achteruit gezet Welk gebied vertoont in de grafiek een niet-uniforme positieve versnelling?
Welk gebied vertoont in de grafiek een niet-uniforme positieve versnelling?  Kunstmatig fotosynthesesysteem krijgt efficiëntieverbetering van grafeen
Kunstmatig fotosynthesesysteem krijgt efficiëntieverbetering van grafeen Nanorobotica openen de bloed-hersenbarrière, hoop bieden op nieuwe hersenbehandelingen
Nanorobotica openen de bloed-hersenbarrière, hoop bieden op nieuwe hersenbehandelingen Is waterstofbromide polair of niet -polair?
Is waterstofbromide polair of niet -polair?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

