
Wetenschap
Kobaltsulfaat wordt blauw met NaOH:chemische reactie uitgelegd
1. Eerste oplossing:
* Kobaltsulfaat (CoSO₄) in oplossing bestaat als roze gehydrateerde kobalt(II)-ionen ([Co(H₂O)₆]²⁺).
2. NaOH toevoegen:
*Als je NaOH toevoegt, reageren de hydroxide-ionen (OH⁻) uit NaOH met de gehydrateerde kobalt(II)-ionen.
3. Complexe ionenvorming:
* Deze reactie zorgt ervoor dat een deel van de watermoleculen rond het kobalt(II)-ion worden vervangen door hydroxide-ionen. Dit resulteert in de vorming van een blauw tetraëdrisch complexion:[Co(OH)₄]²⁻.
4. Kleurverandering:
* Het kleurverschil tussen het roze gehydrateerde kobalt(II)-ion en het blauwe tetraëdrische complexe ion is te wijten aan de verandering in de coördinatieomgeving rond het kobaltatoom. De verschillende liganden (water versus hydroxide) beïnvloeden de manier waarop het kobaltatoom licht absorbeert en uitzendt.
Samengevat:
De toevoeging van NaOH aan de kobaltsulfaatoplossing veroorzaakt een kleurverandering van roze naar blauw omdat dit leidt tot de vorming van een blauw tetraëdrische complexe ion, [Co(OH)₄]²⁻, door enkele watermoleculen rond het kobalt(II)-ion te vervangen door hydroxide-ionen.
 Wordt water de universele opgeloste stof genoemd omdat het veel stoffen oplost?
Wordt water de universele opgeloste stof genoemd omdat het veel stoffen oplost?  Wat is de meest voorkomende vaste vloeistof of gas voor niet -metalen elementen?
Wat is de meest voorkomende vaste vloeistof of gas voor niet -metalen elementen?  Onderzoekers beschouwen de complexiteit van het bioprinten van meercellige weefsels
Onderzoekers beschouwen de complexiteit van het bioprinten van meercellige weefsels Heeft een verbinding een chemische samenstelling?
Heeft een verbinding een chemische samenstelling?  Wanneer gassen warmte verliezen, ze in vloeistoffen?
Wanneer gassen warmte verliezen, ze in vloeistoffen?
 Nieuw commentaar op het beroemde artikel Warning to Humanity brengt wereldwijde ongelijkheden aan het licht
Nieuw commentaar op het beroemde artikel Warning to Humanity brengt wereldwijde ongelijkheden aan het licht Zeespiegelstijging heeft complexe gevolgen:studie
Zeespiegelstijging heeft complexe gevolgen:studie Emissies van nanodeeltjes stijgen met 30 procent wanneer auto's met flexbrandstof overschakelen van bio naar fossiel
Emissies van nanodeeltjes stijgen met 30 procent wanneer auto's met flexbrandstof overschakelen van bio naar fossiel Gemeentelijk afvalwater kan worden gebruikt om ziekten op te sporen in UH-onderzoek
Gemeentelijk afvalwater kan worden gebruikt om ziekten op te sporen in UH-onderzoek Menselijk din verdrinkt de natuur stil,
Menselijk din verdrinkt de natuur stil,
Hoofdlijnen
- Cellen die geen gameten produceren, worden genoemd?
- Bevat een genenpool de genen van individuen die zich niet kunnen voortplanten?
- Worden enzymen ongewijzigd door de reacties waaraan ze deelnemen?
- Hoe zou osmose de groei van bacteriën in een open pot honing beïnvloeden?
- Hoe is fosforylering belangrijk in een signaaltransductiecascade?
- Wat is echt een coole bacterie?
- Een dodelijke schimmel die het witte-neussyndroom veroorzaakt, kan een achilleshiel hebben, studie onthult
- Wat voor soort spieren zijn langwerpig gerangschikt in vellen en bevatten meerdere kernen?
- In Eukaryotes wordt ATP voornamelijk geproduceerd in en vrijgegeven uit?
- Supersnelle methode voor keramische productie zou de deur kunnen openen naar AI-gestuurde materiaalontdekking

- Het jaar voorspellen in de chemie

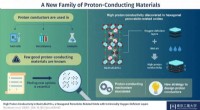
- Nieuwe geleiders met een hoog protonengehalte met inherent zuurstofarme lagen openen een duurzame toekomst
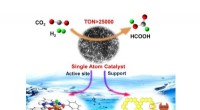
- Katalysator met één atoom gebaseerd op homogeen katalyse-prototype voor CO2-transformatie
- Nieuwe inzichten in het faalmechanisme van lithium-ionbatterijen

 Wat is een rotsdeeltje dat overleeft door de atmosfeer van de aarde?
Wat is een rotsdeeltje dat overleeft door de atmosfeer van de aarde?  Waar is de Gene ST2 voor verantwoordelijk voor?
Waar is de Gene ST2 voor verantwoordelijk voor?  Hoe u vlakglas perfect om hoeken buigt
Hoe u vlakglas perfect om hoeken buigt Welke structuur ontwikkelt zich tot het ruggenmerg van gewervelde dieren?
Welke structuur ontwikkelt zich tot het ruggenmerg van gewervelde dieren?  Hoe wordt het zonnestelsel bestudeerd?
Hoe wordt het zonnestelsel bestudeerd?  Kyawthuite:het zeldzaamste mineraal ooit ontdekt, slechts één keer op aarde gevonden
Kyawthuite:het zeldzaamste mineraal ooit ontdekt, slechts één keer op aarde gevonden  Wanneer een student de snelheid van een rollende bal drie keer meet. Ze voegt metingen toe en verdeelt door 3. Welke hoeveelheid heeft berekend?
Wanneer een student de snelheid van een rollende bal drie keer meet. Ze voegt metingen toe en verdeelt door 3. Welke hoeveelheid heeft berekend?  Wie zijn de immigranten die om humanitaire redenen naar de VS komen, en hoe kunnen zij worden ondersteund?
Wie zijn de immigranten die om humanitaire redenen naar de VS komen, en hoe kunnen zij worden ondersteund?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

