
Wetenschap
Meest gemakkelijk geoxideerde metalen:locatie op het periodiek systeem uitgelegd
* Elektropositiviteit: Metalen in dit gebied hebben een grote neiging elektronen te verliezen en positief geladen ionen (kationen) te worden. Dit komt door hun lage ionisatie-energieën en grote atoomstralen.
* Metallic karakter: Metalen in deze regio vertonen een sterk metaalachtig karakter. Dit betekent dat ze losjes vastgehouden elektronen hebben die gemakkelijk beschikbaar zijn voor oxidatie.
De gemakkelijkst te oxideren metalen zijn specifiek:
* Alkalimetalen (Groep 1): Lithium (Li), natrium (Na), kalium (K), rubidium (Rb), cesium (Cs) en frankium (Fr).
* Aardalkalimetalen (Groep 2): Beryllium (Be), magnesium (Mg), calcium (Ca), strontium (Sr), barium (Ba) en radium (Ra).
Uitzonderingen:
* Overgangsmetalen: Hoewel sommige overgangsmetalen zeer reactief zijn, zijn andere beter bestand tegen oxidatie vanwege hun variërende elektronenconfiguraties en d-orbitale interacties.
Belangrijke opmerking: Het oxidatiepotentieel wordt beïnvloed door factoren zoals:
* pH: De zuurgraad of basiciteit van de omgeving kan de oxidatiesnelheid aanzienlijk beïnvloeden.
* Temperatuur: Hogere temperaturen bevorderen in het algemeen oxidatiereacties.
* Aanwezigheid van oxidatiemiddelen: De aanwezigheid van oxidatiemiddelen zoals zuurstof of halogenen kan het oxidatieproces versnellen.
 Waarom schudt Texas?
Waarom schudt Texas? Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën
Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën Satellietgegevens met open toegang maken het volgen van seizoensgebonden bevolkingsbewegingen mogelijk
Satellietgegevens met open toegang maken het volgen van seizoensgebonden bevolkingsbewegingen mogelijk Wat zijn de 8 ecosystemen?
Wat zijn de 8 ecosystemen?  Hoe ambitieuze doelen te stellen voor duurzame landbouw?
Hoe ambitieuze doelen te stellen voor duurzame landbouw?
Hoofdlijnen
- Afrikaanse gewassen bieden een voedzame, glutenvrije oplossing
- Welk type sporen produceert Selanginella?
- Wat is cyberchondrie?
- Uitleg van celspecialisatie
- Geef koala's een eerlijke kans om te overleven
- Lysosoomverdeling:waar zijn ze het meest overvloedig aanwezig in het lichaam?
- Wat is de naam gegeven aan gebieden in plantencellen die zetmeel- en pigmentmoleculen opslaan?
- Nieuwe uitweg:onderzoekers laten zien hoe stamcellen de bloedbaan verlaten
- Wat is het verschil tussen eukaryotische en prokaryotische cellen?
- Nieuw inzicht in hoe stamcellen interageren met borstkankercellen
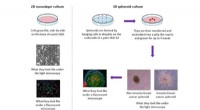
- Keramische membranen scheiden kleine organische moleculen met een molecuulmassa van 200 Dalton

- Ethyleensensor kan helpen bij het bewaken van de gezondheid van planten
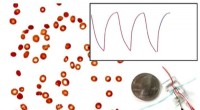
- Onderzoekers ontwikkelen nieuwe methode om snel, betrouwbaar monitoren van sikkelcelziekte
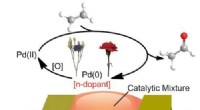
- Tellurium maakt het verschil

 Wat is de evenwichtige chemische vergelijking voor magnesium en zwavel?
Wat is de evenwichtige chemische vergelijking voor magnesium en zwavel?  Welke wetenschappen bestuderen de overblijfselen van het menselijk leven?
Welke wetenschappen bestuderen de overblijfselen van het menselijk leven?  Wat is de laag van zon die verantwoordelijk is voor productie enorme hoeveelheid energie?
Wat is de laag van zon die verantwoordelijk is voor productie enorme hoeveelheid energie?  Wat is de orbitale periode van een object met betrekking tot sterren die worden genoemd?
Wat is de orbitale periode van een object met betrekking tot sterren die worden genoemd?  Wat is een niet-nulgetal?
Wat is een niet-nulgetal?  Solderen hoe werkt
Solderen hoe werkt  Waarom heb je plotselinge uitbarstingen van energie wanneer zijn uitgeput?
Waarom heb je plotselinge uitbarstingen van energie wanneer zijn uitgeput?  Welke structuren worden gebruikt voor het signaleren van directe cellen?
Welke structuren worden gebruikt voor het signaleren van directe cellen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

