
Wetenschap
Wat zijn enkele covalente magnesiumverbindingen?
* magnesiumchloride (mgcl₂): Dit is eigenlijk een ionische verbinding, maar het kan in een covalente vorm in de gasfase bestaan.
* magnesiumoxide (MGO): Dit is ook meestal ionisch, maar vertoont een covalent karakter vanwege het hoge elektronegativiteitsverschil tussen magnesium en zuurstof.
* magnesiumnitride (mg₃n₂): Deze verbinding is ionisch maar heeft een covalent karakter.
* magnesiumhydride (MGH₂): Deze verbinding is meestal ionisch, maar heeft een covalent karakter, waardoor het een nuttig waterstofopslagmateriaal is.
Covalente verbindingen van magnesium met niet -metalen:
* magnesiumbromide (mgbr₂): Een covalente verbinding in de gasfase.
* magnesiumjodide (mgi₂): Een covalente verbinding in de gasfase.
* magnesiumsulfide (mgs): Een covalente verbinding in de gasfase, maar het vertoont een ionisch karakter in vaste toestand.
* magnesium selenide (MGSE): Een covalente verbinding in de gasfase.
* magnesium telluride (mgte): Een covalente verbinding in de gasfase.
Het is belangrijk op te merken dat het covalente karakter van deze verbindingen over het algemeen zwak is. Magnesium is een zeer elektropositief element en het elektronegativiteitsverschil ervan met de meeste niet -metalen is significant, wat leidt tot voornamelijk ionische binding.
Onder bepaalde omstandigheden, zoals in de gasfase of in bepaalde chemische reacties, kan het covalente karakter van deze verbindingen echter prominenter worden.
 Het Zwarte Woud en klimaatverandering
Het Zwarte Woud en klimaatverandering Zou je een tunnel dwars door het middelpunt van de aarde kunnen graven?
Zou je een tunnel dwars door het middelpunt van de aarde kunnen graven?  Model voorspelt stedelijke ontwikkeling en broeikasgassen zullen stedelijke overstromingen aanwakkeren
Model voorspelt stedelijke ontwikkeling en broeikasgassen zullen stedelijke overstromingen aanwakkeren Onderzoekers boren diep om te begrijpen waarom de aardbeving op Sumatra zo hevig was
Onderzoekers boren diep om te begrijpen waarom de aardbeving op Sumatra zo hevig was Aanloop naar vulkaanuitbarsting in Galapagos, in zeldzaam detail vastgelegd
Aanloop naar vulkaanuitbarsting in Galapagos, in zeldzaam detail vastgelegd
Hoofdlijnen
- Hoe fittere vissen meer mensen kunnen voeden te midden van voedselonzekerheid
- Dodelijke bacteriën tonen dorst naar menselijk bloed:onderzoek schetst het fenomeen bacterieel vampirisme
- Verloren of uitgestorven? Onderzoek wijst uit dat het bestaan van meer dan 500 diersoorten onzeker blijft
- Een genetisch materiaal vormt een chromosoom dat?
- Een nieuw begrip van hoe cellen zichzelf verdedigen tegen bacteriële porievormende toxines
- Kunnen golden retrievers langer leven? Onderzoekers vinden genen die verband houden met een lang leven in het ras
- Hoe kun je beter begrijpen wat ervoor zorgt dat een virus wint tijdens de overdracht?
- Wat zijn de 3 soorten sociale wetenschappers?
- Kan plastic gemaakt worden van algen?
- Onderzoekers ontdekken betaalbare methode voor productie van transparante zonnecellen
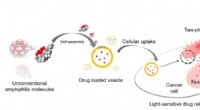
- Nieuwe technologie voor de levering van geneesmiddelen tegen kanker op aanvraag
- Platform optimaliseert het ontwerp van nieuwe, afstembare katalytische systemen

- Koolhydraten vastleggen
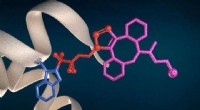
- Nieuwe technologie voor eiwitbioconjugatie en structurele proteomics
 Wat voor soort energietransformatie komt voor als een plafondventilator wordt ingeschakeld?
Wat voor soort energietransformatie komt voor als een plafondventilator wordt ingeschakeld?  Zachte bollen nestelen zich in een enigszins verrassende structuur
Zachte bollen nestelen zich in een enigszins verrassende structuur  Wat gebeurt er als carbonaatmineralen in contact komen met zoutzuur?
Wat gebeurt er als carbonaatmineralen in contact komen met zoutzuur?  Smartphone-sensoren kunnen cannabishigh detecteren en hebben de potentie om vroegtijdig in te grijpen
Smartphone-sensoren kunnen cannabishigh detecteren en hebben de potentie om vroegtijdig in te grijpen Wat komt er na harde schijven?
Wat komt er na harde schijven?  ALMA onderzoekt DeeDee, een verre, zwak lid van ons zonnestelsel
ALMA onderzoekt DeeDee, een verre, zwak lid van ons zonnestelsel Expert legt uit hoe steden de hitte kunnen verslaan door beter te bouwen
Expert legt uit hoe steden de hitte kunnen verslaan door beter te bouwen  Wie ontdekte elastische potentiële energie?
Wie ontdekte elastische potentiële energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

