
Wetenschap
Elektronendichtheid in watermoleculen:de rol van zuurstof begrijpen
* De elektronegativiteit van zuurstof: Zuurstof is aanzienlijk elektronegatiever dan waterstof. Dit betekent dat het een sterkere aantrekkingskracht heeft op gedeelde elektronen in de covalente bindingen.
* Elektronenverdeling: De gedeelde elektronen in de O-H-bindingen brengen meer tijd dichter bij het zuurstofatoom door, waardoor een gedeeltelijke negatieve lading op de zuurstof ontstaat en een gedeeltelijke positieve lading op de waterstofatomen.
* Eenzame paren: Zuurstof heeft ook twee vrije elektronenparen, die niet betrokken zijn bij de binding, maar bijdragen aan de algehele elektronendichtheid rond het zuurstofatoom.
Door deze ongelijke verdeling van elektronen ontstaat een polair molecuul met een gebied met een hogere elektronendichtheid (negatieve pool) rond de zuurstof en een gebied met een lagere elektronendichtheid (positieve pool) rond de waterstofatomen.
 Een beter duurzaam maandverband
Een beter duurzaam maandverband Virtual reality-systemen gebruiken om scheikunde in 3D te onderwijzen
Virtual reality-systemen gebruiken om scheikunde in 3D te onderwijzen Wat is het beperkende reagens wanneer natriumhydroxide en koperchloride reageren?
Wat is het beperkende reagens wanneer natriumhydroxide en koperchloride reageren?  Waarom worden de volumes van aardolieproducten omgezet naar 15 graden Celsius en niet naar een andere temperatuur?
Waarom worden de volumes van aardolieproducten omgezet naar 15 graden Celsius en niet naar een andere temperatuur?  Hoeveel elektronen in Carbon-16?
Hoeveel elektronen in Carbon-16?
 Hoe kustgemeenschappen te helpen bij het opbouwen van weerbestendigheid
Hoe kustgemeenschappen te helpen bij het opbouwen van weerbestendigheid Gegevens van Chinese Fengyun meteorologische satellieten beschikbaar voor wereldwijde wetenschappelijke toepassingen van het aardsysteem
Gegevens van Chinese Fengyun meteorologische satellieten beschikbaar voor wereldwijde wetenschappelijke toepassingen van het aardsysteem Het kapitalisme doodt de populaties wilde dieren in de wereld, niet de mensheid
Het kapitalisme doodt de populaties wilde dieren in de wereld, niet de mensheid Verbeterde secundaire waas door emissiereductie tijdens COVID-19-lockdown in China
Verbeterde secundaire waas door emissiereductie tijdens COVID-19-lockdown in China Het probleem van plasticvervuiling kan grotere gevolgen hebben dan we denken
Het probleem van plasticvervuiling kan grotere gevolgen hebben dan we denken
Hoofdlijnen
- Eerste in zijn soort live-beeldvorming leidt tot belangrijke ontdekkingen in de manier waarop cellen weefsels patrooneren
- Wat staat ook bekend als celsoep?
- Ouderlijke ervaring helpt toekomstige generaties zebravissen omgaan met ongunstige omgevingen
- Waarom denk je dat cytokinese in het middenplane zich meestal voordoet?
- Hoe eet Rhizopus?
- Hoe een calciumgevoelig eiwit multitaskt
- Welke structurele kenmerken karakteriseren prokaryoten?
- Welke tak van wetenschapsiabetes hoort erbij?
- Naar welke twee systemen behoren de testes en eierstokken?
- Verbetering van methoden voor het afleveren van genen

- Een dag om de favoriete eenheid van scheikunde te vieren:de mol. Maar wat is een mol?

- 3D-geprinte eiwitten presteren beter dan bestaande flexibele elektronicamaterialen

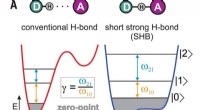
- Experimenten met bifluoride-ionen tonen bewijs van hybride bindingen
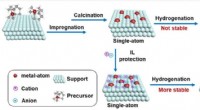
- Wetenschappers ontwikkelen strategie om afzonderlijke atomen te stabiliseren met ionische vloeistof als elektronische stabilisator
 Galileo beweerde dat de zon niet op aarde draaide?
Galileo beweerde dat de zon niet op aarde draaide?  Hoe ruikt steenkool?
Hoe ruikt steenkool?  Hoe kunt u informatie verzamelen van geostationaire sattelieten?
Hoe kunt u informatie verzamelen van geostationaire sattelieten?  Welk type milieuwetenschapper zal waarschijnlijk de effecten chemische morsen op het milieu bestuderen?
Welk type milieuwetenschapper zal waarschijnlijk de effecten chemische morsen op het milieu bestuderen?  Nieuwe vorm van koolstof prikkelt met vooruitzichten voor elektronica
Nieuwe vorm van koolstof prikkelt met vooruitzichten voor elektronica Een toename van de concentratie van ATP Een spiercel is direct resultaat welke levensfunctie?
Een toename van de concentratie van ATP Een spiercel is direct resultaat welke levensfunctie?  Hoe een Chinese telraam te gebruiken
Hoe een Chinese telraam te gebruiken  Wat je moet weten over de eerste testvlucht van het grote ruimteschip van SpaceX
Wat je moet weten over de eerste testvlucht van het grote ruimteschip van SpaceX
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

