
Wetenschap
Inzicht in de aantrekking van water en zuurstof:Van der Waals-krachten
1. Van der Waals dwingt:
* Dit zijn zwakke aantrekkingen op korte afstand die ontstaan als gevolg van tijdelijke fluctuaties in de elektronenverdeling rond moleculen.
* Hoewel zuurstof een niet-polair molecuul is, ervaart het nog steeds tijdelijke, vluchtige momenten van ongelijkmatige elektronenverdeling, waardoor tijdelijke dipolen ontstaan.
*Deze tijdelijke dipolen kunnen vervolgens tijdelijke dipolen in naburige watermoleculen veroorzaken, wat tot een zwakke aantrekkingskracht leidt.
2. Door dipool geïnduceerde dipoolinteracties:
* Watermoleculen zijn polair, wat betekent dat ze een permanente scheiding van lading hebben, met een positief uiteinde (waterstofatomen) en een negatief uiteinde (zuurstofatoom).
* Deze permanente dipool in water kan een tijdelijke dipool in het zuurstofmolecuul veroorzaken, ook al is deze niet-polair.
* Het positieve uiteinde van het watermolecuul wordt aangetrokken door het tijdelijk negatieve uiteinde van het zuurstofmolecuul, en omgekeerd.
Over het algemeen resulteert de combinatie van deze krachten in een zwakke aantrekkingskracht tussen water- en zuurstofmoleculen. Het is echter belangrijk op te merken dat deze aantrekkingskrachten aanzienlijk zwakker zijn dan de sterke waterstofbruggen die tussen watermoleculen onderling bestaan.
Hier is een vereenvoudigde analogie:
Stel je watermoleculen voor als kleine magneten met een positief en negatief uiteinde. Zuurstofmoleculen zijn als niet-gemagnetiseerde metalen voorwerpen. Hoewel de metalen voorwerpen niet sterk aan elkaar blijven kleven, kunnen ze vanwege het geïnduceerde magnetische veld zwak door de magneten worden aangetrokken.
 Aanpassingen van een Macaroni-pinguïn
Aanpassingen van een Macaroni-pinguïn  Ecologieteam ontdekt dat bladafval langzamer afbreekt bij warme temperaturen
Ecologieteam ontdekt dat bladafval langzamer afbreekt bij warme temperaturen Wetenschappers volgen gigantische oceaanvortex vanuit de ruimte
Wetenschappers volgen gigantische oceaanvortex vanuit de ruimte Orkaandelta raast aan land op door storm geteisterde zuidkust VS
Orkaandelta raast aan land op door storm geteisterde zuidkust VS Microbiële gemeenschappen hebben een seizoensverandering doorgemaakt
Microbiële gemeenschappen hebben een seizoensverandering doorgemaakt
Hoofdlijnen
- Indringende vraag:Moet de samenleving reproductieve technologieën reguleren?
- Osmose en celmembranen:waterbeweging begrijpen
- Welke organismen hebben nooit cellen met celwanden?
- Wat voor soort suiker is geen glucose?
- Human Heart Science Projects
- Organismen die twee verschillende allelen hebben voor een eigenschap?
- Welke rol speelt cytokinese tijdens de celcyclus?
- Bijen en vlinders gaan achteruit in westelijk en zuidelijk Noord-Amerika
- Heeft de vroege stijging van het zuurstofgehalte op aarde de evolutie van meercellig leven ondersteund – of onderdrukt?
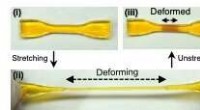
- Zelfgroeiende materialen die sterker worden als reactie op kracht
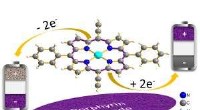
- Natuurlijk molecuul om de prestaties van elektroden voor oplaadbare batterijen te verbeteren
- Carbon black gerecycled uit autobanden

- Voor fotokatalysatoren, de tand des tijds doorstaan betekent een perfecte partner vinden

- Studie ontrafelt hoe microben een belangrijke stof produceren die wordt gebruikt om kanker te bestrijden
 Is zonne-energie een vorm van natuurwetenschap?
Is zonne-energie een vorm van natuurwetenschap?  Wat zijn de voor- en nadelen van het gebruik van grafieken in wiskunde?
Wat zijn de voor- en nadelen van het gebruik van grafieken in wiskunde?  Eigenschappen van magneten & elektromagneten
Eigenschappen van magneten & elektromagneten Wat is de fysica van een lasertaggeweer?
Wat is de fysica van een lasertaggeweer?  Facebook-aandelen kaatsen terug naar pre-schandaalniveau
Facebook-aandelen kaatsen terug naar pre-schandaalniveau Waarom hebben de terrestrische planeten niet ringen?
Waarom hebben de terrestrische planeten niet ringen?  Een nieuw begrip van hoe glucose je dik maakt
Een nieuw begrip van hoe glucose je dik maakt  Wat gebruiken vleermuizen voor energie?
Wat gebruiken vleermuizen voor energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

