
Wetenschap
Polaire versus niet-polaire moleculen:een uitgebreide gids
1. Teken de Lewis-structuur:
* Identificeer het centrale atoom: Dit is meestal het minst elektronegatieve atoom in het molecuul.
* Tel de totale valentie-elektronen: Tel de valentie-elektronen van alle atomen in het molecuul bij elkaar op.
* Verbind de atomen met enkele bindingen: Plaats het centrale atoom in het midden en verbind het met de andere atomen.
* Volledige octetten: Voeg alleenstaande elektronenparen toe aan de buitenste atomen (behalve waterstof) om aan de octetregel te voldoen (acht elektronen rond elk atoom).
2. Bepaal de moleculaire geometrie:
* Gebruik de VSEPR-theorie: De Valence Shell Electron Pair Repulsion (VSEPR)-theorie helpt de vorm van moleculen te voorspellen. Het stelt dat elektronenparen rond een centraal atoom elkaar afstoten en proberen de afstand tussen hen te maximaliseren.
* Gemeenschappelijke geometrieën:
* Lineair: Twee elektronenparen rond het centrale atoom (bijvoorbeeld CO2).
* Trigonaal vlak: Drie elektronenparen (bijvoorbeeld BF3).
* Tetraëdrische: Vier elektronenparen (bijvoorbeeld CH4).
* Trigonaal piramidaal: Drie bindingsparen en één alleenstaand paar (bijvoorbeeld NH3).
* Gebogen: Twee bindingsparen en twee alleenstaande paren (bijvoorbeeld H2O).
3. Analyseer de bindingspolariteit:
* Elektronegativiteit: Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen in een binding aan te trekken.
* Polaire bindingen: Als het elektronegativiteitsverschil tussen twee gebonden atomen significant is (groter dan 0,4), wordt de binding als polair beschouwd. Het meer elektronegatieve atoom zal een gedeeltelijke negatieve lading hebben (δ-), en het minder elektronegatieve atoom zal een gedeeltelijke positieve lading hebben (δ+).
4. Bepaal de moleculaire polariteit:
* Symmetrische moleculen: Als een molecuul een symmetrische geometrie heeft en alle bindingen niet-polair zijn, is het molecuul niet-polair. Dit komt omdat de bindingsdipolen elkaar opheffen.
* Asymmetrische moleculen: Als een molecuul een symmetrische geometrie heeft maar polaire bindingen bevat, of als het molecuul een asymmetrische geometrie heeft, is het molecuul polair. Dit komt omdat de bindingsdipolen elkaar niet opheffen en resulteren in een netto dipoolmoment.
Voorbeelden:
* CO2: Lineaire geometrie, symmetrische, niet-polaire bindingen (verschil in elektronegativiteit is klein). Niet-polair molecuul .
* H2O: Gebogen geometrie, asymmetrische, polaire bindingen (significant elektronegativiteitsverschil tussen zuurstof en waterstof). Polair molecuul .
* CH4: Tetraëdrische geometrie, symmetrische, niet-polaire bindingen (klein elektronegativiteitsverschil tussen koolstof en waterstof). Niet-polair molecuul .
Belangrijkste punten:
* Polariteit is een cruciale factor die de fysische en chemische eigenschappen van een molecuul beïnvloedt, inclusief het kookpunt, de oplosbaarheid en de reactiviteit.
* Bedenk dat zelfs als een molecuul polaire bindingen bevat, het nog steeds niet-polair kan zijn als de geometrie ervan symmetrisch is.
 Waarom zijn metaallegeringen een voorbeeld van een fysieke verandering en geen chemische verandering?
Waarom zijn metaallegeringen een voorbeeld van een fysieke verandering en geen chemische verandering?  Wat is het verschil tussen fysische eigenschappen en chemische eigenschappen?
Wat is het verschil tussen fysische eigenschappen en chemische eigenschappen?  Welke ester vormt wanneer ethylalcohol en mierenzuur reageren?
Welke ester vormt wanneer ethylalcohol en mierenzuur reageren?  Welke stof heeft het hoogste smeltpunt?
Welke stof heeft het hoogste smeltpunt?  Chemicaliën van boerenvelden waar stromen ze niet aan?
Chemicaliën van boerenvelden waar stromen ze niet aan?
Hoofdlijnen
- Wat zou gebeuren, zijn reproductieve cellen waren diploïd?
- Waarom wordt de cel binnengevallen door het virus dat een gastheercel wordt genoemd?
- Hoe bijen hun baby's op natuurlijke wijze vaccineren
- Ambtenaren:walvissen, na een dodelijk jaar, zou kunnen uitsterven
- De vliegsnelheid van vogels is complexer dan eerder werd gedacht
- De peptidoglycan van de bacteriële celwand bevat een koolhydraatmatrix die aan elkaar is gekoppeld, is korte ketens wat?
- Wat is de definitie van en voorbeelden Biomes?
- 7 minder bekende menselijke soorten die met uitsterven zijn bedreigd
- Hoe kun je zien of iets een organisme of plant is?
- Hoe het milieu te helpen:Zet bakolie om in hernieuwbare brandstoffen

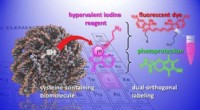
- Nieuwe chemische hulpmiddelen om biomoleculen te wijzigen en te bestuderen
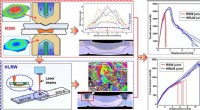
- Onderzoekers verbeteren de mechanische eigenschappen van aluminium/stalen verbindingen
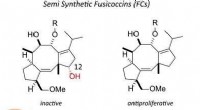
- Bewerkt plantaardig toxine bezit anti-tumor eigenschappen
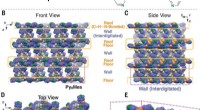
- Materiaal gemaakt van een enkel molecuul vormt zichzelf tot een rooster dat zichzelf kan genezen, gassen opslaan
 overlast buren, gevaarlijke honden:asociaal gedrag heeft invloed op de kwaliteit van leven
overlast buren, gevaarlijke honden:asociaal gedrag heeft invloed op de kwaliteit van leven Waarom kopen mensen al het brood en de melk op voordat een storm losbarst?
Waarom kopen mensen al het brood en de melk op voordat een storm losbarst?  Wat zijn de geologische kenmerken die worden gevonden op transformatieplaatgrenzen?
Wat zijn de geologische kenmerken die worden gevonden op transformatieplaatgrenzen?  Verhoogt het vergroten van de stroom op een draad de magnetische kracht die deze werkt?
Verhoogt het vergroten van de stroom op een draad de magnetische kracht die deze werkt?  De enige stof in de buurt van het oppervlak dat op natuurlijke wijze in de atmosfeer wordt aangetroffen als een vaste vloeistof en gas?
De enige stof in de buurt van het oppervlak dat op natuurlijke wijze in de atmosfeer wordt aangetroffen als een vaste vloeistof en gas?  Welke fysieke eigenschappen kunnen worden gebruikt om twee verschillende stoffen te scheiden?
Welke fysieke eigenschappen kunnen worden gebruikt om twee verschillende stoffen te scheiden?  Is de aarde tijdens haar baan altijd op dezelfde manier gekanteld?
Is de aarde tijdens haar baan altijd op dezelfde manier gekanteld?  Science Project on Nails That Rust
Science Project on Nails That Rust
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

