
Wetenschap
Nieuwe chemische hulpmiddelen om biomoleculen te wijzigen en te bestuderen
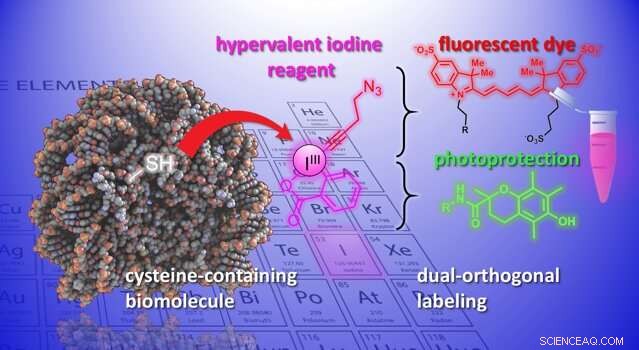
Een illustratie van de chemische reactie die in het onderzoek is ontwikkeld. Krediet:J. Waser/B. Fierz (EPFL)
Het begrijpen van de structuur en het metabolisme van cellen en levende organismen is essentieel voor de ontwikkeling van nieuwe medicijnen en diagnostica. De beschikbaarheid van chemische hulpmiddelen waarmee wetenschappers biomoleculen kunnen bewerken, zoals eiwitten, met resolutie op atoomniveau hebben in hoge mate bijgedragen aan de vooruitgang van de chemische biologie.
Eiwitten zijn macromoleculen die zijn opgebouwd uit een set van twintig chemisch verschillende aminozuren. Een belangrijke benadering om eiwitten te modificeren is om te reageren met het zwavelatoom in het aminozuur cysteïne. Echter, huidige methoden zijn nog steeds problematisch in termen van efficiëntie, selectiviteit, en stabiliteit van het eindproduct (het "adduct").
Nutsvoorzieningen, de laboratoria van Jérôme Waser en Beat Fierz van EPFL's Institute of Chemical Sciences and Engineering hebben een nieuwe methode ontwikkeld voor het modificeren van cysteïnes op peptiden en eiwitten. De methode maakt gebruik van een groep zeer reactieve organische moleculen, de ethynylbenziodoxolonen (EBX's). Wat EBX's zeer reactief maakt, is dat ze een jodiumatoom bevatten dat aan drie substituentgroepen is gebonden. Deze niet-natuurlijke situatie leidt tot een hoge reactiviteit in deze zogenaamde "hypervalente jodium"-reagentia.
Voor de eerste keer, de onderzoekers waren in staat om een eenvoudig biomolecuul-EBX-adduct te genereren terwijl hun reactieve jodiumgroep in het uiteindelijke molecuul bleef. De reactie kan gemakkelijk worden uitgevoerd door een niet-deskundige onder standaard fysiologische omstandigheden.
Het eindproduct zijn eiwit-hypervalente jodiumreagenschimeren die kunnen fungeren als dubbele bevestigingspunten voor twee nieuwe chemische groepen, het openen van nieuwe mogelijkheden voor de studie van biologische processen.
"Een nieuwe functionaliteit kan worden geïntroduceerd via 'klikchemie, ' een gevestigde reactie in de chemische biologie, ", zegt Waser. "Met behulp van een palladiumkatalysator, een andere selectieve modificatie kan worden bereikt bij het reactieve jodiumatoom - wat we een 'biorthogonale' functionaliteit zouden noemen, zoals het in de natuur niet bestaat." Het introduceren van dergelijke exotische reactieve groepen in biomoleculen is momenteel een van de belangrijkste instrumenten in de chemische biologie, omdat het de studie van biologische processen mogelijk maakt zonder ze te verstoren.
De wetenschappers demonstreerden het potentieel van de methode door een diverse reeks chemische groepen in biomoleculen te introduceren. Bijvoorbeeld, de wetenschappers gebruikten de dubbele handgreep om tegelijkertijd een fluorescerende kleurstof en een fotobeschermende groep in een neuropeptide te bevestigen. Door ze te combineren, wordt de fotostabiliteit van de kleurstof verbeterd, en maakt hoge resolutie mogelijk, single-molecule beeldvorming van moleculaire interacties.
Naast peptiden, ze veranderden verder kleine eiwitten, en zelfs grote eiwit-DNA-complexen, zogenaamde nucleosomen. Terwijl nucleosomen het genoom organiseren, door ze te labelen met fluorescerende kleurstoffen, kunnen ze worden gevolgd om te ontcijferen hoe de natuur genexpressie reguleert.
"Wat we hier hebben ontwikkeld, is een nieuwe methode voor het modificeren van eiwitten op basis van fundamentele studies van chemische reactiviteit, " zegt Fierz. "We hebben het al gebruikt om histonen te modificeren, en voerden fluorescentie-experimenten uit op levende cellen. Met deze voorbeelden we hebben de basis gelegd voor een beter begrip van biologische processen."
De studie is gepubliceerd in Chemo vandaag.
 Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld
Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld Hoe helpt Spectroscopy elementen te identificeren?
Hoe helpt Spectroscopy elementen te identificeren?  Samenwerking tussen studenten zorgt voor nieuwe inzichten in hoogwaardig drinkwater tegen lagere kosten
Samenwerking tussen studenten zorgt voor nieuwe inzichten in hoogwaardig drinkwater tegen lagere kosten Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden
Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden Nieuwe techniek maakt snelle en goedkope productie van hoogwaardige circuits mogelijk
Nieuwe techniek maakt snelle en goedkope productie van hoogwaardige circuits mogelijk
 Bosbranden woeden in Griekenland, de geboorteplaats van de Olympische Spelen bedreigen
Bosbranden woeden in Griekenland, de geboorteplaats van de Olympische Spelen bedreigen Afrikaanse post-Covid-plannen moeten prioriteit geven aan klimaat:studie
Afrikaanse post-Covid-plannen moeten prioriteit geven aan klimaat:studie Vitamine b12, en een knock-off-versie, complexe markt creëren voor mariene vitamines
Vitamine b12, en een knock-off-versie, complexe markt creëren voor mariene vitamines Californische oliepijpleiding had een jaar kunnen lekken:onderzoekers
Californische oliepijpleiding had een jaar kunnen lekken:onderzoekers Vermindering van bosbrandgevaar:hier is een idee van gecontroleerde brandwonden dat het proberen waard is
Vermindering van bosbrandgevaar:hier is een idee van gecontroleerde brandwonden dat het proberen waard is
Hoofdlijnen
- Onderzoek toont aan dat honden slimmer zijn dan katten
- Waarom is diffusie belangrijk voor het leven van een cel?
- Bij voetbalsucces draait alles om vaardigheid:studeren
- Dierenartsen verplegen zieke bobcat, breng het terug naar het park waar het nodig is
- Ambtenaren:GGO-muggen zijn geen drugs, EPA-toezicht nodig
- De Pomodoro-techniek:je kunt elke taak 25 minuten per keer aan
- Doel van Cell Lysis Solution
- 10 onderzoeken die compleet bizarre dingen met elkaar verbinden
- Gel elektroforese lezen
- Instant waterreinigingsmethode miljoenen keren beter dan commerciële aanpak

- Tumbleweeds of fibrillen:Tau-eiwitten moeten kiezen
- Synthese van biobased high-performance polyamide uit biogene residuen
- Ontdekking kan leiden tot zelfrijdende robots

- Team creëert microbe om afval om te zetten in nuttige chemicaliën
 Onderzoekers ontwikkelen microscopische theorie van polymeergel
Onderzoekers ontwikkelen microscopische theorie van polymeergel Wanneer een aerobatic vliegtuig ondersteboven vliegt,
Wanneer een aerobatic vliegtuig ondersteboven vliegt,  De frontlinieverdediging van het immuunsysteem bevriest bacteriën in hun sporen
De frontlinieverdediging van het immuunsysteem bevriest bacteriën in hun sporen Momentum remmen in de diepe ruimte
Momentum remmen in de diepe ruimte Mineraal in maanmeteoriet suggereert dat er ooit water op de maan was
Mineraal in maanmeteoriet suggereert dat er ooit water op de maan was De waarde van beroepslicenties neemt af in de online wereld
De waarde van beroepslicenties neemt af in de online wereld Eerste experimentele waarneming van nieuw type verstrengeling in een 2D-kwantummateriaal
Eerste experimentele waarneming van nieuw type verstrengeling in een 2D-kwantummateriaal Astronomen ontdekken de meest röntgenlichtgevende quasar met hoge roodverschuiving
Astronomen ontdekken de meest röntgenlichtgevende quasar met hoge roodverschuiving
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

