
Wetenschap
Zilver en zwavelzuur:de reactie (of het gebrek daaraan) begrijpen
* Silver's positie in de reactiviteitsreeks: Zilver is een minder reactief metaal vergeleken met waterstof. Het bevindt zich onder waterstof in de reactiviteitsreeks. Dit betekent dat het minder waarschijnlijk is dat het waterstof uit zijn verbindingen, inclusief zwavelzuur, verdringt.
* Vorming van een beschermende laag: Wanneer zilver in contact komt met zwavelzuur, vormt zich op het oppervlak een dun laagje zilversulfaat (Ag₂SO₄). Deze laag fungeert als een beschermende barrière en voorkomt verdere reactie.
Er zijn echter enkele omstandigheden waaronder zilver kan reageren met zwavelzuur:
* Heet, geconcentreerd zwavelzuur: Als je heet, geconcentreerd zwavelzuur gebruikt, is de reactie mogelijk. Het hoge temperatuur en geconcentreerde zuur kan de beschermende laag overwinnen en leiden tot de vorming van zilversulfaat en zwaveldioxide (SO₂).
* Aanwezigheid van oxidatiemiddelen: Als je een oxidatiemiddel, zoals salpeterzuur, aan het zwavelzuur toevoegt, kan dit helpen het zilver te oxideren en de reactie te bevorderen. Dit komt omdat het oxidatiemiddel de verwijdering van elektronen uit zilver vergemakkelijkt, waardoor de kans groter is dat het reageert.
De algehele reactie met heet, geconcentreerd zwavelzuur kan als volgt worden weergegeven:
2Ag(s) + 2H₂SO₄(l) → Ag₂SO₄(s) + SO₂(g) + 2H₂O(l)
Het is belangrijk op te merken dat:
* Zilver reageert veel langzamer met zwavelzuur vergeleken met de reactie van reactievere metalen.
* De reactie vereist specifieke omstandigheden, waardoor deze in alledaagse situaties minder vaak voorkomt.
Laat het me weten als je nog vragen hebt!
 62,13 kg Al omzetten in mol?
62,13 kg Al omzetten in mol?  Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen
Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen Wat is de chemische naam van 2H2O zijn gemeenschappelijke naam?
Wat is de chemische naam van 2H2O zijn gemeenschappelijke naam?  Wat is een evenwichtige vergelijking voor KNO3 Nabr en CAS?
Wat is een evenwichtige vergelijking voor KNO3 Nabr en CAS?  Wat deden de alchemisten dat een verbetering was ten opzichte van de Griekse methode om materie te ontdekken?
Wat deden de alchemisten dat een verbetering was ten opzichte van de Griekse methode om materie te ontdekken?
 Waarom mogen kinderen niet stemmen? Een deskundige ontkracht de tegenargumenten
Waarom mogen kinderen niet stemmen? Een deskundige ontkracht de tegenargumenten  Studie onderzoekt hoe onzekerheid de politieke tolerantie kan beïnvloeden
Studie onderzoekt hoe onzekerheid de politieke tolerantie kan beïnvloeden  Waarom het niet altijd onze schuld is als we voor ongezond voedsel kiezen
Waarom het niet altijd onze schuld is als we voor ongezond voedsel kiezen  Aanwijzing voor condensatie legt uit hoe planten veranderende herfsttemperaturen waarnemen
Aanwijzing voor condensatie legt uit hoe planten veranderende herfsttemperaturen waarnemen  Iran:decennia van niet-duurzaam watergebruik hebben meren doen opdrogen en vernietiging van het milieu veroorzaakt
Iran:decennia van niet-duurzaam watergebruik hebben meren doen opdrogen en vernietiging van het milieu veroorzaakt
Hoofdlijnen
- Waaruit bestaat de celwand van plantencellen?
- Droogte decimeert de belangrijkste katoenoogst in Texas
- Wat zijn de basisstructurele eenheden van DNA- en RNA -moleculen?
- Soorten individuen die seksueel reproduceren, hebben de neiging om variatie te missen waar onwaar?
- Wie was de wetenschapper die de evolutie theorie maakt?
- Wat is immunohistochemie?
- Planten worden toleranter als ze in symbiose met schimmels leven
- Is prokaryote of eukaryote een bacterieplantencel diercel?
- Wordt glycogenese een proces dat onmiddellijk na de maaltijd onmiddellijk voorkomt?
- Ionische zonnecel kan on-demand waterontzilting bieden;

- Nieuwe chemie maakt verbeteringen aan magische medicijnen gemakkelijker

- De wetenschap achter wasmiddelen:hoe ze de spanning op het wateroppervlak verminderen

- Een veelbelovende strategie om de activiteit in antimicrobiële peptiden te verhogen
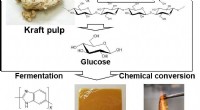
- De hoogste hittebestendige kunststof ooit is ontwikkeld uit biomassa
 Hoe wordt een rivierbron gevormd?
Hoe wordt een rivierbron gevormd?  Onderzoek onthult zelfgenoegzaamheid over klimaatverandering in heel Europa
Onderzoek onthult zelfgenoegzaamheid over klimaatverandering in heel Europa Identificeer het hormoon dat wordt uitgescheiden in een deel van het menselijk lichaam dat gal sap produceert?
Identificeer het hormoon dat wordt uitgescheiden in een deel van het menselijk lichaam dat gal sap produceert?  De ionisatie -energie voor natrium is 496 kjmol elektronenaffiniteit chloor -349 Wat de enthalpie?
De ionisatie -energie voor natrium is 496 kjmol elektronenaffiniteit chloor -349 Wat de enthalpie?  Satellieten om treinen te volgen en de veiligheid op het spoor te bevorderen
Satellieten om treinen te volgen en de veiligheid op het spoor te bevorderen Exploderende experimenten voor kinderen
Exploderende experimenten voor kinderen  Wanneer zien we een volle maan aan de nachtelijke hemel?
Wanneer zien we een volle maan aan de nachtelijke hemel?  Neurale netwerken onder de loep nemen
Neurale netwerken onder de loep nemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

