
Wetenschap
De wetenschap achter wasmiddelen:hoe ze de spanning op het wateroppervlak verminderen
Door Athena Hessong Bijgewerkt op 24 maart 2022
Kwangmoozaa/iStock/GettyImages
Wasmiddelmoleculen hebben een zeer slimme eigenschap:het ene uiteinde is hydrofiel, of waterminnend, en het andere uiteinde hydrofoob, oftewel afgestoten door water. Door deze dubbele aard kan wasmiddel zowel water als olie aantrekken, waardoor het uw wasgoed kan reinigen. Het is ook zeer effectief in het verminderen van de oppervlaktespanning van water door watermoleculen uit elkaar te duwen met het hydrofobe uiteinde van het wasmiddelmolecuul.
Watermoleculen en oppervlaktespanning
Watermoleculen en oppervlaktespanning
Water heeft unieke eigenschappen waardoor het aan het oppervlak ‘plakkerig’ wordt. Elk individueel watermolecuul heeft één groot zuurstofatoom en twee kleinere waterstofatomen. De waterstofatomen hebben een licht positieve lading, waardoor het hele watermolecuul polair is. Net als kleine magneten trekken de waterstofatomen de zuurstofatomen van andere watermoleculen aan, waardoor tijdelijke waterstofbruggen in het water ontstaan.
Elk watermolecuul ervaart vanuit elke richting een aantrekkingskracht van andere watermoleculen, maar watermoleculen aan het oppervlak hebben geen moleculen boven het oppervlak die eraan kunnen trekken. Deze watermoleculen hebben meer trekkracht van het water eronder dan van het oppervlak erboven. Door dit krachtverschil worden de watermoleculen aan het oppervlak dichter bij elkaar gepakt dan ze zich in de vloeistof bevinden. De dunne, dichte laag moleculen veroorzaakt het fenomeen dat oppervlaktespanning wordt genoemd.
Wasmiddel en zeep
Wasmiddel en zeep
Wasmiddel en zeep zijn chemisch vergelijkbaar, behalve de olie die erin zit. Veel zepen gebruiken natuurlijke vetten, terwijl wasmiddelen geraffineerde aardolie gebruiken. Zeep- en wasmiddelmoleculen hebben twee uiteinden die fungeren als een brug tussen watermoleculen en vetmoleculen (vet). Hierdoor kan de zeep of het wasmiddel zich aan het vet van een vuile vaat hechten en het andere uiteinde van het wasmiddelmolecuul gebruiken om zich vast te hechten aan het water dat moet worden weggespoeld.
Wasmiddel en zeep breken de oppervlaktespanning
Wasmiddel en zeep breken de oppervlaktespanning
De twee uiteinden van wasmiddelmoleculen zorgen ervoor dat het de oppervlaktespanning van water kan doorbreken. Het uiteinde van het wasmiddelmolecuul dat zich aan vet (vet) hecht, stoot watermoleculen af. Het staat bekend als hydrofoob, wat ‘watervrezend’ betekent. Door te proberen weg te bewegen van de watermoleculen, duwen de hydrofobe uiteinden van de wasmiddelmoleculen zich naar het oppervlak. Dit verzwakt de waterstofbruggen die de watermoleculen aan het oppervlak bij elkaar houden. Het resultaat is een breuk in de oppervlaktespanning van het water.
 Het perfecte getij nabootsen om wetlands aan de kust te beschermen tegen stijgende zeespiegels
Het perfecte getij nabootsen om wetlands aan de kust te beschermen tegen stijgende zeespiegels Baanbrekende fossiele voetafdrukken opgegraven in Kenia onthullen belangrijke inzichten in het gedrag van vroege mensachtigen
Baanbrekende fossiele voetafdrukken opgegraven in Kenia onthullen belangrijke inzichten in het gedrag van vroege mensachtigen  Amerikaanse projecties over de door droogte getroffen Colorado-rivier worden erger
Amerikaanse projecties over de door droogte getroffen Colorado-rivier worden erger VN bevestigt 18,3C recordhitte op Antarctica
VN bevestigt 18,3C recordhitte op Antarctica EPA verklaart Denver, noordelijk Front Range, tot ernstige overtreders van luchtkwaliteitsnormen omdat de staat er niet in slaagt smog te verminderen
EPA verklaart Denver, noordelijk Front Range, tot ernstige overtreders van luchtkwaliteitsnormen omdat de staat er niet in slaagt smog te verminderen
Hoofdlijnen
- Wat is een web van eiwit gevonden in celcytoplasma?
- Wetenschappers ontdekken hoe dodelijke schimmel zichzelf beschermt
- Wat is het tegenovergestelde van meiose?
- Welke organellen worden alleen aangetroffen in plantencellen en waarom?
- Wat betekent vertakkende evolutie?
- Welke twee organismen delen een mutualistisch partnerschap in de vorming van mycorrhizae?
- Hoe wordt het genoemd wanneer bladeren groeien in cirkelvormige patronen rond delen van een stengel?
- Hoe genoctrooien werken
- Zijn de subeenheden van een celfunctie onafhankelijk?
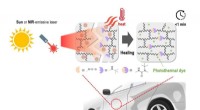
- Hoe biologies hardst werkende pigmenten en MOF's het klimaat kunnen redden

- Studie onderzoekt de chemische stof GenX in water:is het anders dan andere PFAS?

- Beschermend coatingmateriaal herstelt zichzelf in 30 minuten bij blootstelling aan zonlicht
- Onderzoek naar roamingreacties om nieuw licht te werpen op atmosferische moleculen

- Peptide-vingerafdruk maakt eerdere diagnose van de ziekte van Alzheimer mogelijk

 Een kracht geeft een massa van 2,0 kg een versnelling van 5,0 op het niveau van het niveau Wat is de toegepast op massa?
Een kracht geeft een massa van 2,0 kg een versnelling van 5,0 op het niveau van het niveau Wat is de toegepast op massa?  Franse rechtbank beveelt Twitter om kleine lettertjes te wijzigen na privacyzaak
Franse rechtbank beveelt Twitter om kleine lettertjes te wijzigen na privacyzaak Spaanse vulkaanuitbarsting sluit luchthaven gebied nog steeds gespannen
Spaanse vulkaanuitbarsting sluit luchthaven gebied nog steeds gespannen NASA's Terra-satelliet ziet vuur en rook van verwoestende bosbranden in Australië
NASA's Terra-satelliet ziet vuur en rook van verwoestende bosbranden in Australië Hoe te berekenen Gemiddelde leeftijd
Hoe te berekenen Gemiddelde leeftijd  Een laser op nanoschaal gemaakt van goud en zinkoxide
Een laser op nanoschaal gemaakt van goud en zinkoxide Wat is het genotype van twee zwarte heterozygote cavia?
Wat is het genotype van twee zwarte heterozygote cavia?  Airbus zegt in gesprek met Emirates over vitale A380-deal
Airbus zegt in gesprek met Emirates over vitale A380-deal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

