
Wetenschap
Natriumchloride versus suiker:elektrische geleidbaarheid begrijpen
Natriumchloride (NaCl):
* Ionische verbinding: Natriumchloride is een ionische verbinding. Dit betekent dat het wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* Dissociatie in water: Wanneer natriumchloride in water oplost, breken de ionische bindingen en worden de ionen omgeven door watermoleculen. Deze ionen kunnen nu onafhankelijk binnen de oplossing bewegen.
* Geleidbaarheid: Door de aanwezigheid van vrije, mobiele ionen kan de oplossing elektriciteit geleiden. Wanneer een elektrische potentiaal wordt aangelegd, bewegen de positief geladen ionen naar de negatieve elektrode (kathode) en bewegen de negatief geladen ionen naar de positieve elektrode (anode). Deze ladingsstroom vormt een elektrische stroom.
Suiker (sucrose):
* Covalente verbinding: Suiker is een covalente verbinding. De atomen worden bij elkaar gehouden door gedeelde elektronen en vormen sterke, neutrale moleculen.
* Geen vrije ionen: Wanneer suiker oplost in water, valt het niet uiteen in ionen. De suikermoleculen blijven intact en dragen geen elektrische lading.
* Geen geleidbaarheid: Omdat er geen vrije ionen zijn die de lading kunnen dragen, geleidt een suikeroplossing geen elektriciteit.
Samengevat:
Het vermogen van een oplossing om elektriciteit te geleiden hangt af van de aanwezigheid van vrije, mobiele ionen. Ionische verbindingen zoals natriumchloride dissociëren in ionen in oplossing, waardoor geleiding mogelijk is. Covalente verbindingen zoals suiker vormen geen ionen in oplossing en geleiden daarom geen elektriciteit.
 Condensatie -kernen zijn betrokken bij de vorming?
Condensatie -kernen zijn betrokken bij de vorming?  De elektronen in de binding tussen waterstof en fluor worden sterker aangetrokken tot welk atoom?
De elektronen in de binding tussen waterstof en fluor worden sterker aangetrokken tot welk atoom?  On-demand glas is om de hoek
On-demand glas is om de hoek Water helpt bij de onverwachte en ultrasnelle synthese van collageenachtig synthetisch poly-L-proline
Water helpt bij de onverwachte en ultrasnelle synthese van collageenachtig synthetisch poly-L-proline Waar krijg je meer voorbeelden voor Michael Addition Reaction?
Waar krijg je meer voorbeelden voor Michael Addition Reaction?
Hoofdlijnen
- Op welke organnelles zijn de mitochondria afhankelijk?
- Waarom is het nuttig om elk van uw monsters te verteren met twee verschillende restrictie -enzymen?
- Wat zijn Holandric Genen?
- Welke organismen die op andere organismen leven en er niets voor teruggeven zijn?
- Een groep gelijk uitziende organismen die kunnen kruisen en vruchtbare nakomelingen kunnen produceren, wordt genoemd?
- Voorbeelden van een recessief allel
- Hoe is biotechnologie mogelijk schadelijk geweest voor het milieu?
- Tetrads begrijpen in de microbiologie:vorming, functie en betekenis
- Welke soorten cellen die de cortex vormen in planten?
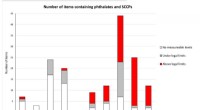
- Gifstoffen in oud speelgoed een obstakel voor circulaire economie
- Vormen discrete moleculen bindingen? Onderzoek naar binding in discrete stoffen

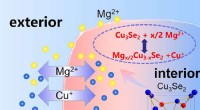
- Koperion ontsluit magnesiumpotentieel in batterijen van de volgende generatie
- Onderzoekers rapporteren nieuwe techniek voor het ontdooien van oppervlakken

- Video:Hortensia's, de vreemde van kleur veranderende bloemen

 Structurele inzichten in kleine bacteriële harpoenen
Structurele inzichten in kleine bacteriële harpoenen In het hart van Hartley-2, een komeet van een nieuw ras?
In het hart van Hartley-2, een komeet van een nieuw ras?  Waarom sommige rode wijnen droog smaken
Waarom sommige rode wijnen droog smaken Onderzoekers gebruikten dieselvervuiling om te begrijpen hoe roet ijs vormt in cirruswolken
Onderzoekers gebruikten dieselvervuiling om te begrijpen hoe roet ijs vormt in cirruswolken  Hoe op te vallen, in hagedisstijl
Hoe op te vallen, in hagedisstijl  Welke vormen van energie zijn er een spijker te hameren?
Welke vormen van energie zijn er een spijker te hameren?  Hoe kun je uitleggen hoe levende dingen direct en indirect energie van de zon halen?
Hoe kun je uitleggen hoe levende dingen direct en indirect energie van de zon halen?  Is het uitgebrande of uitgebrande gloeilamp?
Is het uitgebrande of uitgebrande gloeilamp?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

