
Wetenschap
De elektronen in de binding tussen waterstof en fluor worden sterker aangetrokken tot welk atoom?
Dit is waarom:
* elektronegativiteit: Fluor is het meest elektronegatieve element op het periodiek systeem. Elektronegativiteit is het vermogen van een atoom om elektronen naar zichzelf aan te trekken in een chemische binding.
* Polaire covalente binding: Het verschil in elektronegativiteit tussen waterstof en fluor is significant, wat resulteert in een polaire covalente binding. Dit betekent dat de elektronen niet gelijk worden gedeeld tussen de atomen.
* Gedeeltelijke ladingen: Het fluoratoom zal een gedeeltelijke negatieve lading hebben (Δ-) omdat het de gedeelde elektronen sterker aantrekt. Het waterstofatoom heeft een gedeeltelijke positieve lading (Δ+).
Dit verschil in elektronegativiteit en de resulterende ongelijke delen van elektronen maakt de H-F-binding polair.
 Noem twee factoren die worden gebruikt om een stof te identificeren met behulp van papierchromatografie?
Noem twee factoren die worden gebruikt om een stof te identificeren met behulp van papierchromatografie?  Doorbraak in de medicamenteuze chemie kan leiden tot betere geneesmiddelen
Doorbraak in de medicamenteuze chemie kan leiden tot betere geneesmiddelen Wat zijn de drie belangrijkste gassen die warmte vangen?
Wat zijn de drie belangrijkste gassen die warmte vangen?  Hoe wordt een atoomspectra geproduceerd?
Hoe wordt een atoomspectra geproduceerd?  Microfluidics helpt ingenieurs om virale infectie in realtime te bekijken
Microfluidics helpt ingenieurs om virale infectie in realtime te bekijken
 35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel
35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel Komt het broeikaseffect alleen op aarde voor?
Komt het broeikaseffect alleen op aarde voor?  Near Earth Objects - wat staat ons te wachten?
Near Earth Objects - wat staat ons te wachten?  Hoe een verbeterde groene infrastructuur in de binnenstad de volksgezondheid kan verbeteren
Hoe een verbeterde groene infrastructuur in de binnenstad de volksgezondheid kan verbeteren Nieuwe database:waterbronnen in 43 staten bevatten potentieel onveilige chemische niveaus
Nieuwe database:waterbronnen in 43 staten bevatten potentieel onveilige chemische niveaus
Hoofdlijnen
- Een nieuw quarantaineschema zou het risico op herintroductie van hondsdolheid in de EU na de Russische invasie kunnen verminderen, zo blijkt uit onderzoek
- Sommige commerciële ontsmettingsmiddelen werken mogelijk niet zo goed tegen het norovirus als oorspronkelijk werd gedacht
- Welk model beschrijft het kenmerk van celmembraan?
- Wat zijn de twee gemeenschappelijke namen voor DNA -structuur?
- Hoe malaria het immuunsysteem bedriegt?
- Wetenschappers lokaliseren jaloezie in de monogame geest
- Wat is Mendels -verhouding voor dominante tot recessieve eigenschappen?
- Is de term cerebrale dominantie het halfrond aan dat dominant is voor taal?
- Het opsporen van een cellulaire 'kortsluiting' werpt licht op hoe bepaalde ziekten beginnen
- Wegwerpmaskers kunnen worden gebruikt om beton te verbeteren

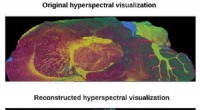
- Computationele methode zorgt voor snellere massaspectrometriebeeldvorming met hoge resolutie
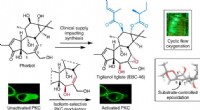
- Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
- Aanpassingen van zeezoogdieren aan een laag zuurstofgehalte bieden een nieuw perspectief op COVID-19

- Machine learning gaat dieper in op katalysatorinteracties om de ontwikkeling van materialen te versnellen
 Hoe een orkaan bosbranden veroorzaakte in de Florida Panhandle
Hoe een orkaan bosbranden veroorzaakte in de Florida Panhandle Wat het doel van mitochondria in een cel?
Wat het doel van mitochondria in een cel?  Welke planeten kan niet worden gezien met het blote oog?
Welke planeten kan niet worden gezien met het blote oog?  Welk voorbeeld beschrijft een geërfde eigenschap die niet kan worden bepaald door het observeren van het individu?
Welk voorbeeld beschrijft een geërfde eigenschap die niet kan worden bepaald door het observeren van het individu?  Hoe voorspellen de Azteken eclipsen?
Hoe voorspellen de Azteken eclipsen?  Hoe het periodiek systeem te onthouden
Hoe het periodiek systeem te onthouden Gebruik van citroenzuurpoeder
Gebruik van citroenzuurpoeder  Theetijd krijgt smaakboost van dunne film, onzuiver water
Theetijd krijgt smaakboost van dunne film, onzuiver water
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

