
Wetenschap
Verbranding van niet-metalen:chemische vergelijkingen en voorbeelden
Niet-metaal + zuurstof → Niet-metaaloxide
De specifieke producten en coëfficiënten zullen echter variëren afhankelijk van het specifieke betrokken niet-metaal. Hier zijn enkele voorbeelden:
1. Verbranding van koolstof:
C(s) + O₂(g) → CO₂(g)
2. Verbranding van zwavel:
S(s) + O₂(g) → SO₂(g)
3. Verbranding van fosfor:
4P(s) + 5O₂(g) → 2P₂O₅(s)
4. Verbranding van waterstof:
2H₂(g) + O₂(g) → 2H₂O(g)
Belangrijke opmerking: Bij de verbranding van niet-metalen ontstaan vaak zure oxiden. Zwaveldioxide (SO₂) lost bijvoorbeeld op in water en vormt zwavelzuur (H₂SO₃).
Algemene opmerkingen:
* Exotherme reactie: Verbranding is altijd een exotherme reactie, waarbij warmte en licht vrijkomen.
* Zuurstofbehoefte: Alle verbrandingsreacties vereisen zuurstof als reactant.
* Productvorming: De producten van de verbranding van niet-metalen zijn gewoonlijk oxiden van het niet-metaal.
* Onvolledige verbranding: In sommige gevallen kan een onvolledige verbranding optreden, wat resulteert in de vorming van koolmonoxide (CO) of andere onvolledig geoxideerde producten.
 Laat de spermaraces beginnen
Laat de spermaraces beginnen Onderzoekers creëren morphing-kristallen die worden aangedreven door waterverdamping
Onderzoekers creëren morphing-kristallen die worden aangedreven door waterverdamping Toepassing van groene chemieprincipes op ijzerkatalyse
Toepassing van groene chemieprincipes op ijzerkatalyse  Rutherford theoretiseerde dat atomen een dicht positief centrum of kern hebben hoe het bewijs voor deze conclusie wordt geïllustreerd in geanimeerd goud-foil-experiment?
Rutherford theoretiseerde dat atomen een dicht positief centrum of kern hebben hoe het bewijs voor deze conclusie wordt geïllustreerd in geanimeerd goud-foil-experiment?  De schadelijke effecten van zuren en basen begrijpen
De schadelijke effecten van zuren en basen begrijpen
 Wetenschappers vinden ontbrekend stuk in voorspellingen van gletsjersmelt
Wetenschappers vinden ontbrekend stuk in voorspellingen van gletsjersmelt Wat is het kenmerk van een goede gemeenschap?
Wat is het kenmerk van een goede gemeenschap?  Eerste ontdekking van microplastics uit water dat vastzit op bladeren van planten
Eerste ontdekking van microplastics uit water dat vastzit op bladeren van planten Onderzoekers verklaren ammoniakverdeling in de bovenste atmosfeer van de aarde
Onderzoekers verklaren ammoniakverdeling in de bovenste atmosfeer van de aarde Hoe beïnvloeden mensen landvormen?
Hoe beïnvloeden mensen landvormen?
Hoofdlijnen
- Wat zijn de kenmerken van blad- en uiencellen van wangcellen?
- Hoeveel allelen heeft een gamete voor elke eigenschap en is het haploïd of diploïd?
- Oude scheikunde kan verklaren waarom levende wezens ATP gebruiken als de universele energievaluta
- Waarom kunnen twee vergelijkbare soorten niet dezelfde niche hebben?
- Welke plantencelstructuren lijken te ontbreken in de cellen van een uienlamp?
- Wat is de Thermosophere -laag?
- In dierlijke protisten worden de korte draadachtige structuren die zich uitstrekken van celmembraan genoemd?
- Wat is reproductieve capaciteit?
- Hoe organiseren wetenschappers?
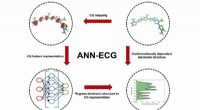
- Nieuwe benadering van moleculaire modellering kan de ontwikkeling van nieuwe organische materialen voor elektronica versnellen
- Ongekende 3D-beelden van de anatomie van het menselijk oor voor gehoorherstel
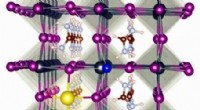
- Een complete set van energieniveauposities van alle primaire metaalhalogenideperovskieten
- Wereldprimeur:nieuw polymeer gaat wandelen als het verlicht is

- DNA programmeren om medicijnen tegen kanker af te leveren

 Wat is er een samengestelde naam voor 7h2o?
Wat is er een samengestelde naam voor 7h2o?  Is Mannitol Salt Agar -complex of synthetisch?
Is Mannitol Salt Agar -complex of synthetisch?  Wat is een metafoor voor chloroplast?
Wat is een metafoor voor chloroplast?  Plaats overtroeft race niet als voorspeller van opsluiting
Plaats overtroeft race niet als voorspeller van opsluiting Wat zijn de energietransfers in een op batterijen bediende radio?
Wat zijn de energietransfers in een op batterijen bediende radio?  Nieuwe studie van landelijk India benadrukt de rol van de schoonmoeder bij het beperken van de sociale netwerken van vrouwen
Nieuwe studie van landelijk India benadrukt de rol van de schoonmoeder bij het beperken van de sociale netwerken van vrouwen Hoe verandert de vorm van cellen tijdens osmose en diffusie?
Hoe verandert de vorm van cellen tijdens osmose en diffusie?  Klimaatverandering maakt herhaling Dust Bowl twee keer zo waarschijnlijk
Klimaatverandering maakt herhaling Dust Bowl twee keer zo waarschijnlijk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

