
Wetenschap
Rutherford theoretiseerde dat atomen een dicht positief centrum of kern hebben hoe het bewijs voor deze conclusie wordt geïllustreerd in geanimeerd goud-foil-experiment?
De setup
* Alpha -deeltjes: Stel je voor dat een stroom van kleine, positief geladen deeltjes (alfa -deeltjes) wordt afgevuurd als kogels uit een bron.
* Goudfolie: Een dun vel goudfolie werkt als het doelwit.
* Detectorscherm: Rondom de gouden folie is een scherm bedekt met een materiaal dat gloeit wanneer hij wordt geraakt door alfa -deeltjes.
De animatie
1. De meeste deeltjes gaan dwars door: De animatie toont het grootste deel van de alfa -deeltjes die dwars door de gouden folie passeren en het scherm er direct achter slaan. Dit suggereert dat het grootste deel van het atoom lege ruimte is.
2. Sommige deeltjes zijn afgebogen: Een klein aantal deeltjes wordt echter afgebogen, waardoor hun pad verandert terwijl ze door de folie passeren. Sommigen worden enigszins afgebogen, terwijl anderen worden afgebogen onder veel grotere hoeken.
3. Een paar deeltjes worden achteruit afgebogen: De meest opvallende observatie is dat enkele deeltjes bijna direct achteruit worden afgebogen, alsof ze van een vast object waren gestuiterd.
de interpretatie van Rutherford
Rutherford interpreteerde deze resultaten als volgt:
* Lege ruimte: Het feit dat de meeste deeltjes door de goudfolie gaan, suggereert dat atomen meestal lege ruimte zijn.
* Dichte, positieve kern: De afbuiging van sommige deeltjes duidt op de aanwezigheid van een klein, dicht, positief geladen gebied in het atoom, dat hij de kern noemde.
* afstoting: De grote deflecties en achterwaartse verstrooiing treden op omdat alfa -deeltjes (positief) worden afgestoten door de positieve kern. Deze afstoting is veel sterker wanneer het alfa -deeltje dicht bij de kern komt.
De animatie belicht
* De animatie moet de relatieve afmetingen van de kern en het atoom benadrukken, waaruit blijkt dat de kern veel kleiner is.
* Het zou ook de verschillende trajecten van de alfa -deeltjes moeten tonen - rechte paden, lichte afbuigingen en grote deflecties.
* De animatie moet duidelijk aantonen dat een zeer klein percentage deeltjes significante afbuiging ervaart.
Conclusie
Het goudfolie -experiment, zoals gevisualiseerd in de animatie, bracht een revolutie teweeg in ons begrip van het atoom. Het model van Rutherford, gebaseerd op dit bewijs, is nog steeds de basis van ons huidige begrip van de atomaire structuur.
 Wat is de ultieme bron van genetische variatie en basen voor het diversiteitsleven op aarde?
Wat is de ultieme bron van genetische variatie en basen voor het diversiteitsleven op aarde?  Onderzoekers vinden verband tussen media-aandacht voor droogte en huishoudelijke waterbesparing
Onderzoekers vinden verband tussen media-aandacht voor droogte en huishoudelijke waterbesparing Ideeën om te doen voor Science Fair voor vijfde klas
Ideeën om te doen voor Science Fair voor vijfde klas  Rapport:Grote Meren voelen effecten van snelle klimaatopwarming (update)
Rapport:Grote Meren voelen effecten van snelle klimaatopwarming (update) Bosbranden Griekenland:Winden ventilator 2 nieuwe branden buiten Athene
Bosbranden Griekenland:Winden ventilator 2 nieuwe branden buiten Athene
Hoofdlijnen
- Wat zijn de verschillende soorten amoeba?
- Welke twee vormen komen prokaryoten binnen?
- Waarom lijkt het leven zo vergelijkbaar met Valens?
- Honingbijen stemmen om te beslissen over nestplaatsen – waarom we zouden moeten luisteren
- De levenscyclus van Gymnosperms
- Uit welke taal zijn de meeste voorwaarden voor organen voortgekomen?
- BigH1 - de belangrijkste histon voor mannelijke vruchtbaarheid
- Om te groeien en te overleven hebben cellen informatie nodig uit hun DNA-voedingsomgeving. Wanneer een cel echter te groot wordt, wat doet deze dan?
- Wat is de taak van mitochondriën in een dierlijke cel?
- Russische wetenschappers ontwikkelen een slim sorptiemiddel voor waterzuivering

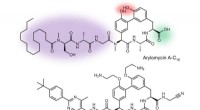
- Gemodificeerde arylomycine blijkt effectief te zijn tegen resistente bacteriën
- Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen

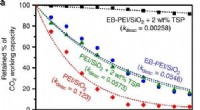
- Onderzoekers produceren 50x stabieler adsorbens
- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

 Wat is de massa stamcellen die in de eerste paar dagen na de bevruchting wordt genoemd, produceert?
Wat is de massa stamcellen die in de eerste paar dagen na de bevruchting wordt genoemd, produceert?  Sorry, Elon Musk, maar het is nu duidelijk dat kolonisatie van Mars onwaarschijnlijk is - en een slecht idee
Sorry, Elon Musk, maar het is nu duidelijk dat kolonisatie van Mars onwaarschijnlijk is - en een slecht idee Wanneer Butaan met zuurstof reageert, wat doet de temperatuur in de omgeving?
Wanneer Butaan met zuurstof reageert, wat doet de temperatuur in de omgeving?  Waarom wordt natuurkunde beschouwd als het centrale deel van de wetenschap?
Waarom wordt natuurkunde beschouwd als het centrale deel van de wetenschap?  Ruimtelijke straatkunst
Ruimtelijke straatkunst Hoe heet een enkel helixmolecuul?
Hoe heet een enkel helixmolecuul?  Gebruikt ons lichaam slechts één energiesysteem tegelijk?
Gebruikt ons lichaam slechts één energiesysteem tegelijk?  Kenmerken van het land in het Biome-zoetwaterbiotoestel
Kenmerken van het land in het Biome-zoetwaterbiotoestel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

