
Wetenschap
Zeer reactieve metalen:een uitgebreide gids
Metalen zijn reactiever dan waterstof:
* Groep 1 (Alkalimetalen): Lithium (Li), natrium (Na), kalium (K), rubidium (Rb), cesium (Cs), frankium (Fr)
* Groep 2 (aardalkalimetalen): Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba), Radium (Ra)
* Aluminium (Al)
* Zink (Zn)
* IJzer (Fe)
* Tin (Sn)
* Leiding (Pb)
Waarom zijn ze reactiever?
De reactiviteit van een metaal houdt verband met de neiging ervan om elektronen te verliezen en positieve ionen te vormen. Metalen die reactiever zijn dan waterstof hebben een sterkere neiging om elektronen te verliezen en positieve ionen te vormen in vergelijking met waterstof.
Voorbeeld:
Wanneer een metaal zoals zink reageert met zoutzuur (HCl), verliezen de zinkatomen elektronen en vormen zinkionen (Zn²⁺), terwijl waterstofionen (H⁺) elektronen winnen en waterstofgas (H₂) vormen:
Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g)
Opmerking:
* Edelmetalen (bijvoorbeeld goud, zilver, platina) zijn minder reactief dan waterstof en reageren niet met zuren.
* De reactiviteit van metalen neemt over het algemeen toe naarmate u een groep lager in het periodiek systeem beweegt, en neemt af naarmate u zich door een periode verplaatst.
* Deze reactiviteitsreeks helpt bij het voorspellen van de uitkomst van reacties tussen metalen en zuren.
 Offshore olie- en gasplatforms stoten meer methaan uit dan eerder geschat
Offshore olie- en gasplatforms stoten meer methaan uit dan eerder geschat Franse boeren blokkeren raffinaderijen vanwege import van palmolie
Franse boeren blokkeren raffinaderijen vanwege import van palmolie CO2-uitstoot in ontwikkelde economieën daalt door afnemend gebruik van fossiele brandstoffen en energie
CO2-uitstoot in ontwikkelde economieën daalt door afnemend gebruik van fossiele brandstoffen en energie Is jungle cat alomtegenwoordig of herbivoren?
Is jungle cat alomtegenwoordig of herbivoren?  Na olie:hoe Maleisië en Iran eruit kunnen zien in een toekomst na fossiele brandstoffen
Na olie:hoe Maleisië en Iran eruit kunnen zien in een toekomst na fossiele brandstoffen
Hoofdlijnen
- Hoe worden witte bloedcellen met één grote kern genoemd?
- DNA draagt genetische informatie in zijn?
- Vergelijking voor glucosemetabolisme
- Rode bloedcellen:het zuurstoftoevoersysteem van uw lichaam - wat u moet weten
- De evolutie van slijm:hoe komen we aan al dit slijm?
- Trofeejacht kan uitsterven veroorzaken in een veranderende omgeving
- Maatregelen voor welzijn en duurzaamheid heroverwegen van lokale naar mondiale schaal
- Waar is het DNA in het menselijk lichaam?
- Wat is een catayst?
- Nieuwe diepgaande leerbenadering voorspelt eiwitstructuur op basis van aminozuursequentie
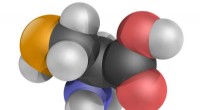
- Onderzoeksteam ontcijfert enzymatische afbraak van suiker uit zeealgen

- Korte totale synthese van ajoen, een biologisch actieve component in olie-extracten van knoflook
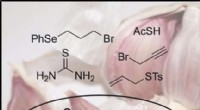
- Licht schijnend op de dynamiek van de aangeslagen toestand in perovskietmaterialen
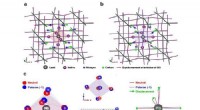
- Een efficiënte benadering van geconjugeerde tetraenen uit butadieen en alkynen
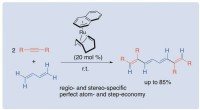
 Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis
Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis Waar wordt ATP het meest efficiënt geproduceerd?
Waar wordt ATP het meest efficiënt geproduceerd?  Een verband leggen tussen luchtvervuiling en dementie
Een verband leggen tussen luchtvervuiling en dementie Hoeveel sneller is een vliegtuig dan de auto?
Hoeveel sneller is een vliegtuig dan de auto?  Nieuwe nanotechnologie zet warmte om in energie wanneer dat het meest nodig is
Nieuwe nanotechnologie zet warmte om in energie wanneer dat het meest nodig is Hoeveelheid O2 en N2 in de lucht?
Hoeveelheid O2 en N2 in de lucht?  Nieuw bewijs voor donkere materie:de staven in sterrenstelsels draaien langzamer dan we dachten
Nieuw bewijs voor donkere materie:de staven in sterrenstelsels draaien langzamer dan we dachten Hoe lang duurt een sterrencyclus?
Hoe lang duurt een sterrencyclus?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

