
Wetenschap
Waarom zijn nobele gassen niet -reactief?
* Elektronenconfiguratie: Atomen streven ernaar om een stabiele elektronenconfiguratie te bereiken, zoals de edelgassen. Dit betekent een volledige buitenste schaal van elektronen, wat de meest stabiele opstelling is.
* valentie -elektronen: De buitenste schaal elektronen, bekend als valentie -elektronen, zijn betrokken bij chemische binding. Nobele gassen hebben een compleet octet (acht valentie -elektronen) in hun buitenste schaal, behalve voor helium, dat een volledig duet heeft (twee valentie -elektronen).
* Het is niet nodig om te binden: Omdat ze al een stabiele elektronenconfiguratie hebben, hoeven edelgassen geen elektronen te krijgen of te verliezen om bindingen met andere atomen te vormen. Dit maakt ze uitzonderlijk niet -reactief.
Samenvattend: Nobele gassen zijn niet -reactief omdat ze een volledige buitenste schaal van elektronen hebben, waardoor ze inherent stabiel en bestand zijn tegen het vormen van chemische bindingen.
 Wat is de verbinding Si3H8?
Wat is de verbinding Si3H8?  Wetenschappers stellen redoxmechanisme voor water-gasverschuivingsreactie voor
Wetenschappers stellen redoxmechanisme voor water-gasverschuivingsreactie voor Welke kleur zou een mengsel van thymolblauw en fenolftaleïne krijgen als natriumhydroxide werd toegevoegd?
Welke kleur zou een mengsel van thymolblauw en fenolftaleïne krijgen als natriumhydroxide werd toegevoegd?  Onderzoekers ontdekken een nieuwe gunstige functie van een oud eiwit
Onderzoekers ontdekken een nieuwe gunstige functie van een oud eiwit Waar vindt de oxidatieroute voor het afbouwen van voedsel in ATP op?
Waar vindt de oxidatieroute voor het afbouwen van voedsel in ATP op?
 Vorming van gletsjermoulin veroorzaakt door snelle afwatering van meren
Vorming van gletsjermoulin veroorzaakt door snelle afwatering van meren Wespennesten identificeren
Wespennesten identificeren Wie definieerde de klimaatverandering?
Wie definieerde de klimaatverandering?  Hard Rock in de diepzee - de weg naar het ontcijferen van biodiversiteit op de zeebodem is steniger dan eerder werd aangenomen
Hard Rock in de diepzee - de weg naar het ontcijferen van biodiversiteit op de zeebodem is steniger dan eerder werd aangenomen Wat is de oorsprong van wolkenkoekoekland?
Wat is de oorsprong van wolkenkoekoekland?
Hoofdlijnen
- Waar haalt het hoornvlies zuurstof vandaan?
- Mitotische celdeling is geïnitieerd in de?
- Waarom hebben de meeste wetenschappers de hypothese van Wegeners afgewezen?
- Uit onderzoek blijkt dat er overeenkomsten zijn tussen de manier waarop duiven het equivalent van woorden leren en de manier waarop kinderen dat doen
- Hoeveel cellen zitten er in de dierencel?
- Wat vereist transcriptie in eukaryoten toevoeging aan RNA -polymerase?
- Welk deel van de ademhaling produceert de meeste ATP?
- Wanneer een gen twee of meer fenotypische eigenschappen regelt?
- Wat is de agronomische classificatie van een aardappel?
- Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn
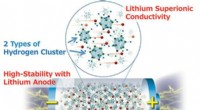
- Hoe biologies hardst werkende pigmenten en MOF's het klimaat kunnen redden

- Nieuwe katalysatormethode belooft beter gebruik van syngas, steenkool

- Wetenschappers vinden een manier om DNA-oppervlaktehybridisatie te versnellen

- Studie onthult een unieke manier van celmigratie op zachte visco-elastische oppervlakken
 Welk vet bevat grote hoeveelheden vetzuur die leidt tot een vermindering van de neiging van de neiging bloedstolsel?
Welk vet bevat grote hoeveelheden vetzuur die leidt tot een vermindering van de neiging van de neiging bloedstolsel?  Is het Atlasgebergte een belangrijke landvorm in de Sahara?
Is het Atlasgebergte een belangrijke landvorm in de Sahara?  Waarom heeft water als ijs een koeleffect?
Waarom heeft water als ijs een koeleffect?  Waar komt nieuwe korst vandaan in de verspreiding van zeebodem?
Waar komt nieuwe korst vandaan in de verspreiding van zeebodem?  Wat transformeert energie in voedselmoleculen in bruikbare energie?
Wat transformeert energie in voedselmoleculen in bruikbare energie?  Hoeveel luchtmoleculen in de atmosfeer?
Hoeveel luchtmoleculen in de atmosfeer?  Naar welke vorm van energie wordt uiteindelijk allemaal veranderd?
Naar welke vorm van energie wordt uiteindelijk allemaal veranderd?  NASA-astronauten arriveren voor Boeings eerste menselijke ruimtevlucht
NASA-astronauten arriveren voor Boeings eerste menselijke ruimtevlucht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

