
Wetenschap
Hoe heeft Atom -onderzoek uitgevoerd door John Dalton Sir Joseph Thomson Ernest Rutherford en Niels Bohr Impact Scientific Thought door de geschiedenis van de wetenschap?
John Dalton (1803):
* Dalton's atomaire theorie: Dalton stelde voor dat elementen zijn samengesteld uit ondeelbare deeltjes die atomen worden genoemd. Deze theorie, gebaseerd op experimentele waarnemingen, vormde een basis voor het begrijpen van chemische reacties en de eigenschappen van materie.
* impact: Dalton's theorie vestigde het concept van atomen als de kleinste eenheid van materie, waardoor het begrip van chemische samenstelling een revolutie teweegbracht en de weg vrij te maken voor verder atoomonderzoek.
J.J. Thomson (1897):
* Ontdekking van het elektron: Thomson ontdekte het elektron, een negatief geladen deeltje dat veel kleiner is dan het atoom. Deze ontdekking daagde het idee van Dalton van ondeelbare atomen uit.
* pruimpuddingmodel: Thomson stelde het "pruimpudding" -model voor, wat suggereert dat het atoom een sfeer van positieve lading was met negatief geladen elektronen ingebed.
* impact: Thomson's ontdekking van het elektron en zijn model veranderde het begrip van de atomaire structuur aanzienlijk, introduceerde het idee van subatomaire deeltjes en effent de weg voor verder onderzoek naar de interne structuur van het atoom.
Ernest Rutherford (1911):
* Nucleair model: Rutherford ontdekte door zijn beroemde gouden folie -experiment de kern, een dichte, positief geladen regio in het midden van het atoom. Hij stelde het nucleaire model voor, wat suggereert dat elektronen rond de kern draaien.
* impact: Het model van Rutherford bracht een revolutie teweeg in het begrip van de atomaire structuur en vestigde de kern als het centrale en meest massale deel van het atoom, verantwoordelijk voor zijn positieve lading. Deze ontdekking legde de basis voor verder atoomonderzoek, inclusief de ontwikkeling van nucleaire fysica.
Niels Bohr (1913):
* Bohr -model: Bohr stelde een model van het atoom voor waar elektronen de kern in specifieke energieniveaus of schalen ronddraaien. Hij legde de lijnspectra van elementen uit door te suggereren dat elektronen tussen energieniveaus konden springen, licht uitzenden of absorberen.
* impact: Het model van Bohr gaf een meer accurate beschrijving van de atomaire structuur dan die van Rutherford en legde de spectrale eigenschappen van elementen uit. Het legde de basis voor de ontwikkeling van de kwantummechanica, een grote doorbraak in de natuurkunde die een revolutie teweegbracht in ons begrip van het atoom en de eigenschappen ervan.
Algehele impact:
Het onderzoek van Dalton, Thomson, Rutherford en Bohr legden de basis voor ons moderne begrip van het atoom. Hun werk leidde tot de ontwikkeling van:
* Moderne chemie: Het concept van atomen en hun eigenschappen maakte de ontwikkeling van moderne chemie mogelijk, inclusief het periodiek systeem en chemische binding.
* kernfysica: Rutherford's ontdekking van de kern opende de deur naar het gebied van de nucleaire fysica, wat leidde tot het begrip van radioactiviteit, nucleaire reacties en kernenergie.
* kwantummechanica: Het werk van Bohr maakte de weg vrij voor de ontwikkeling van de kwantummechanica, die een revolutie teweegbracht in het begrip van materie op atomair en subatomaire niveaus.
Deze ontdekkingen hadden een grote invloed op het wetenschappelijk denken, wat leidde tot vooruitgang op verschillende gebieden en vormden ons begrip van het universum op het meest fundamentele niveau.
 Wetenschappers identificeren de meest urgente problemen van chemicaliën in het milieu
Wetenschappers identificeren de meest urgente problemen van chemicaliën in het milieu Zijn bestaande wetten voldoende om de steeds snellere milieuverandering het hoofd te bieden?
Zijn bestaande wetten voldoende om de steeds snellere milieuverandering het hoofd te bieden? Huizen in Florida geëvacueerd omdat afvalwaterlek een catastrofale overstroming riskeert
Huizen in Florida geëvacueerd omdat afvalwaterlek een catastrofale overstroming riskeert Historische aardbevingen testen Indonesische seismische risicobeoordeling
Historische aardbevingen testen Indonesische seismische risicobeoordeling NASA ziet Irma sterker worden tot orkaan van categorie 5
NASA ziet Irma sterker worden tot orkaan van categorie 5
Hoofdlijnen
- Bij het bestuderen van evolutie betekent de term isolatie één?
- Welke is het enzym zonder eiwit?
- Neurowetenschapper onderzoekt 'Hoe het is om een hond te zijn'
- 3D-röntgentechnologie gebruiken voor de detectie van illegale handel in wilde dieren
- Wat zijn ominivoren en geven voorbeelden?
- Hoe doden aanvullende buitenlandse microben?
- Wat zijn enkele voorbeelden van dierlijke hulpbronnen?
- Een eenvoudig diermodel laat zien hoe omgeving en toestand worden geïntegreerd om gedrag te controleren
- Wat is een kenmerk van kankercellen?
- In-situ inzichten op nanoschaal in de evolutie van vaste elektrolyt-interfaseschillen

- LSU Chemical Engineering onthult nieuwe destillatiekolommen

- Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen

- Lang gehypothetiseerd wondermateriaal van de volgende generatie voor het eerst gemaakt
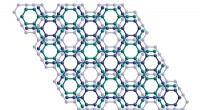
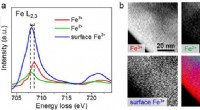
- Efficiënte waterstofconversie door splitsing van water door zonne-energie met behulp van op hematiet-mesocrystal gebaseerde fotoanodes
 Wat is de luchtdichtheid bij 0 C?
Wat is de luchtdichtheid bij 0 C?  Kunnen heterotrofen hun eigen voedsel maken?
Kunnen heterotrofen hun eigen voedsel maken?  Asteroïde komt vrijdag dichtbij:maak je geen zorgen, waren veilig
Asteroïde komt vrijdag dichtbij:maak je geen zorgen, waren veilig Hoe kunt u de grootte en richting van de resulterende kracht berekenen, een object dat wordt opgewerkt door een 4.0N 10N die in dezelfde richting zijn?
Hoe kunt u de grootte en richting van de resulterende kracht berekenen, een object dat wordt opgewerkt door een 4.0N 10N die in dezelfde richting zijn?  Hoe veilig is de Hudson? Wetenschappers testen rivier, Adirondacks naar Ocean
Hoe veilig is de Hudson? Wetenschappers testen rivier, Adirondacks naar Ocean  Hoe zijn de wortels cruciaal om planten te overleven?
Hoe zijn de wortels cruciaal om planten te overleven?  Boek onderzoekt ruig individualisme en de impact ervan op ongelijkheid in Amerika
Boek onderzoekt ruig individualisme en de impact ervan op ongelijkheid in Amerika Aluminium carbonaat bij verwarmde ontbindingen?
Aluminium carbonaat bij verwarmde ontbindingen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

