
Wetenschap
Hoeveel valance -elektronen kunnen atomen van niet -metalen hebben?
Dit is waarom:
* valentie -elektronen Zijn de elektronen in de buitenste schaal van een atoom, en zij zijn degenen die betrokken zijn bij chemische binding.
* niet -metalen bevinden zich aan de rechterkant van het periodiek systeem. Ze hebben de neiging elektronen te krijgen om een stabiel octet (8 valentie -elektronen) te bereiken, zoals de edelgassen.
Voorbeelden:
* zuurstof (O) heeft 6 valentie -elektronen.
* chloor (Cl) heeft 7 valentie -elektronen.
* stikstof (n) heeft 5 valentie -elektronen.
Houd er rekening mee dat er enkele uitzonderingen zijn, zoals waterstof (H) die slechts 1 valentie -elektron hebben. Maar over het algemeen hebben niet -metalen een groot aantal valentie -elektronen.
 Welk type warmteoverdracht kan optreden door transparante stoffen?
Welk type warmteoverdracht kan optreden door transparante stoffen?  Wat is moeilijker om gasvloeistof of vaste stof te comprimeren?
Wat is moeilijker om gasvloeistof of vaste stof te comprimeren?  Wanneer natriumchloride in water wordt opgelost, is de resulterende oplossing geclassificeerd als een?
Wanneer natriumchloride in water wordt opgelost, is de resulterende oplossing geclassificeerd als een?  Is chloor uit de periodiek systeem gevonden in een pool?
Is chloor uit de periodiek systeem gevonden in een pool?  Wat is de chemische stof tegenover zuur?
Wat is de chemische stof tegenover zuur?
 Families uit 8 landen klagen EU aan wegens klimaatverandering
Families uit 8 landen klagen EU aan wegens klimaatverandering Hoe het gebruik van natuurlijke hulpbronnen te verminderen
Hoe het gebruik van natuurlijke hulpbronnen te verminderen Voorbeelden van competitie tussen organismen van dezelfde soort
Voorbeelden van competitie tussen organismen van dezelfde soort Nieuwe soorten oude knaagdieren duiden op wat de oudste graslanden ter wereld zouden kunnen zijn
Nieuwe soorten oude knaagdieren duiden op wat de oudste graslanden ter wereld zouden kunnen zijn  'Ik ben een Mac' - en dan? Onderzoek vindt een manier om de aantrekkingskracht van merkpersoonlijkheid te meten
'Ik ben een Mac' - en dan? Onderzoek vindt een manier om de aantrekkingskracht van merkpersoonlijkheid te meten
Hoofdlijnen
- Archeologie en ecologie geven samen een vollediger beeld van vroegere relaties tussen mens en natuur
- MIT-onderzoeker legt uit hoe ratten denken
- NASA Twins-onderzoek wordt gerepliceerd op Everest
- Is transpiratie een type osmose?
- Hoe werkt het skelet met het ademhalingssysteem?
- Bedwantsen proberen in je vuile was te komen
- Waarom is succinaat dehydrogenase een goed marker -enzym?
- Wat is bemesting in de biologie?
- Wat is het lopende ontdekkingsproces in de wetenschap genoemd?
- Neutronen observeren vitamine B6-afhankelijke enzymactiviteit die nuttig is voor de ontwikkeling van geneesmiddelen
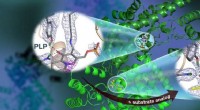
- Chemici ontwikkelen nieuw reagens voor de-elektronisatie
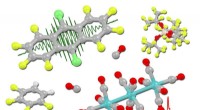
- Wetenschappers synthetiseren een nieuwe stof met antitumorale eigenschappen

- Video:Hoe dieren gloeien

- Kunstmatige zoetstof kan op een dag kankerbehandelingen bieden met minder bijwerkingen
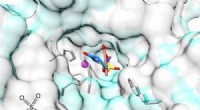
 Wat is de belangrijkste fonograaftype schrijver of gloeilamp?
Wat is de belangrijkste fonograaftype schrijver of gloeilamp?  Boom of grote struik met ronde bladeren en eetbare bruine noten?
Boom of grote struik met ronde bladeren en eetbare bruine noten?  Wat is de chemische formule voor een koolwaterstofverbinding?
Wat is de chemische formule voor een koolwaterstofverbinding?  Welk metaal is erg reactief en onder olie gehouden?
Welk metaal is erg reactief en onder olie gehouden?  Hoe zien sterren eruit via een telescoop en hoe kan hun uiterlijk het beste worden waargenomen?
Hoe zien sterren eruit via een telescoop en hoe kan hun uiterlijk het beste worden waargenomen?  Elon Musks SpaceX gaat $ 500 miljoen ophalen:rapport
Elon Musks SpaceX gaat $ 500 miljoen ophalen:rapport Wat is het klimaat van Walk Two Moons?
Wat is het klimaat van Walk Two Moons?  Wat beperkt het aantal organismen in een omgeving?
Wat beperkt het aantal organismen in een omgeving?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

