
Wetenschap
Wat gebeurt er met de atomen in een vloeistof terwijl deze bevriest?
1. Verlies van energie: Terwijl een vloeistof afkoelt, verliezen de atomen kinetische energie. Dit betekent dat ze langzamer bewegen en minder krachtig trillen.
2. Verminderde afstand: Met minder energie worden de aantrekkelijke krachten tussen atomen dominanter. De atomen beginnen dichter bij elkaar te komen.
3. Vorming van een kristalrooster: In de meeste gevallen, terwijl de vloeistof blijft afkoelen, regelen de atomen zich in een zeer geordende, herhaling van driedimensionaal patroon dat een kristalrooster wordt genoemd. Deze structuur minimaliseert de potentiële energie van het systeem.
4. Verminderde bewegingsvrijheid: In een vaste stof worden de atomen in wezen op hun plaats opgesloten in het kristalrooster. Ze kunnen nog steeds trillen, maar ze kunnen niet vrij van de ene locatie naar de andere bewegen. Dit is wat vaste stoffen hun stijfheid en vaste vorm geeft.
belangrijke opmerkingen:
* Niet alle vloeistoffen bevriezen in kristallijne vaste stoffen. Sommige stoffen, zoals glas, vormen amorfe vaste stoffen waar de atomen op een meer willekeurige, ongeordende manier zijn gerangschikt.
* vriespunt: De specifieke temperatuur waarbij een vloeistof bevriest, wordt het vriespunt genoemd. Dit punt hangt af van de stof en de druk.
* Faseverandering: Het proces van een vloeistof die in een vaste stof wordt, is een faseverandering en het gaat om een verandering in de toestand van materie.
Samenvattend: Vriezen is een proces waarbij atomen in een vloeistof energie verliezen, dichter bij elkaar komen en een meer geordende structuur vormen, wat resulteert in een vaste toestand.
 Wat is de uitgebalanceerde vergelijking voor de verbranding van magnesium?
Wat is de uitgebalanceerde vergelijking voor de verbranding van magnesium?  Waarom is papier een organisch materiaal?
Waarom is papier een organisch materiaal?  Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken?
Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken? Wat gebeurt er als natriumhydroxide wordt toegevoegd aan kopersulfaatoplossing?
Wat gebeurt er als natriumhydroxide wordt toegevoegd aan kopersulfaatoplossing?  Superflexibele elektroluminescente apparaten ontwikkeld
Superflexibele elektroluminescente apparaten ontwikkeld
Hoofdlijnen
- Het is moeilijk om fossiele huid te vinden, maar een zeldzame ontdekking onthult aanwijzingen over de evolutie van water naar land
- 5 mensen die niet begraven kunnen blijven
- Decodering van hondencognitie:machine learning geeft een glimp van hoe het brein van een hond vertegenwoordigt wat het ziet
- Waar komt jouw inktvis vandaan? Hoogstwaarschijnlijk ongereguleerde wateren, volgens een nieuwe internationale studie
- Eerste melding van wondbehandeling door een wild dier met een pijnstillende plant
- Soorten forensische tests
- Wetenschappers zeggen dat een One Health-benadering van plantgezondheid van vitaal belang is voor het bereiken van duurzame wereldwijde voedselzekerheid
- Wanneer wordt het inwendige van de cel als isotoon met de omringende vloeistof beschouwd?
- Hoge nachttemperaturen hebben een negatieve invloed op de productie van koolzaadplanten
- Hete trillende gassen onder de elektronenschijnwerper

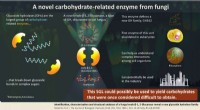
- Nieuwe familie in de buurt:een nieuwe groep glycosidische enzymen
- Gericht op ijzeropname om een nieuwe klasse antibiotica tegen urineweginfecties te creëren
- Teamwetenschap leidt tot doorbraak in kooldioxideomzetting

- Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren

 Het geheim van het volgen van dodelijke infecties? Het zou Mosquito Pee
Het geheim van het volgen van dodelijke infecties? Het zou Mosquito Pee  Haaientelling bereikt eerste 100 riffen:vroege bevindingen van mondiaal onderzoek tonen aan dat bestaande gegevens mogelijk onnauwkeurig zijn
Haaientelling bereikt eerste 100 riffen:vroege bevindingen van mondiaal onderzoek tonen aan dat bestaande gegevens mogelijk onnauwkeurig zijn  Wat is 12 voet en werd tijd geleden in de grond begraven?
Wat is 12 voet en werd tijd geleden in de grond begraven?  10 gekke militaire wapens die echt bestaan
10 gekke militaire wapens die echt bestaan  Wat voor soort conflict kan optreden omdat eigendom?
Wat voor soort conflict kan optreden omdat eigendom?  Vinden zuren of basen sneller?
Vinden zuren of basen sneller?  Gammastraling pulsaties gedetecteerd door de pulsar J0952-0607
Gammastraling pulsaties gedetecteerd door de pulsar J0952-0607 Waarom is de pH -waarde van zout water 8?
Waarom is de pH -waarde van zout water 8?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

