
Wetenschap
Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken?
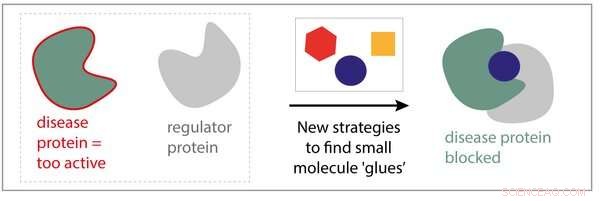
Nieuwe strategieën voor kleine moleculaire lijmen. Credit:Technische Universiteit Eindhoven
Veel van de momenteel beschikbare medicijnen zijn niet specifiek genoeg om complexe ziekten zoals kanker, neurodegeneratieve ziekten en diabetes. In aanvulling, resistentie tegen geneesmiddelen vermindert de effectiviteit van bestaande therapieën. Om deze problemen aan te pakken, biomedisch ingenieur Eline Sijbesma ontwierp kleine moleculen die bepaalde ziekte-eiwitten ontwapenen door ze aan andere eiwitten te lijmen. Deze zouden kunnen leiden tot stabielere en effectievere medicijnen en, onder andere, zou kunnen bijdragen aan een nieuwe therapie voor resistente borstkanker, waarvoor momenteel geen behandeling bestaat. Sijbesma verdedigt haar Ph.D. scriptie op 2 december aan de TU/e.
Als je je de cel voorstelt als de kleinste fabriek van het leven, denk dan aan eiwitten als de machines in deze fabrieken, al het werk doen. Net als bij machines in een productielijn, eiwitten werken niet op zichzelf; ze hebben elkaar nodig om te functioneren. Fysieke interacties tussen eiwitten creëren essentiële signaalnetwerken, waardoor cellen snel en adequaat kunnen reageren op externe signalen. Bij ziekte, vaak functioneert een enkel eiwit niet goed, of te actief is. De activiteit van deze ziektegerelateerde eiwitten kan worden gecorrigeerd door ze stevig te binden aan geneesmiddelen met kleine moleculen die hun normale functie kunnen herstellen. Echter, deze aanpak is niet altijd succesvol en zelfs als dat wel het geval is, zieke cellen vinden vaak manieren om de behandeling te omzeilen.
Twee is beter dan een
Eline Sijbesma, doctoraat student in de onderzoeksgroep Chemische Biologie onder leiding van professor Luc Brunsveld:"In plaats van te focussen op een enkel eiwit en te proberen er een specifiek medicijn voor te vinden, waarom streven we er niet naar om medicijnen te maken die binden aan een complex gevormd door twee eiwitten?" Sijbesma's hypothese is dat als we moleculen kunnen ontwikkelen die de interactie van een eiwit met een ander stabiliseren, we kunnen misschien een ziekte-eiwit 'kleven' aan een 'regulator-eiwit' dat zijn slechte activiteiten voorkomt. Aanvullend, deze moleculen zijn veel selectiever, omdat ze alleen het eiwitcomplex binden, niet de twee individuele eiwitten, waardoor er minder bijwerkingen zijn.
Strak en sterk
Samen met de University of California San Francisco (UCSF) en de Novartis Institutes for Biomedical Research (NIBR), Sijbesma was de pionier van verschillende strategieën voor het ontdekken van geneesmiddelen, waarbij hij gebruik maakte van zeer kleine moleculen (fragmenten) als uitgangspunt. Sijbesma:"We hebben meerdere fragmenten met gewenste eigenschappen geïdentificeerd en op een slimme manier samengevoegd, om één nieuw molecuul te vormen met nog betere eigenschappen. We toonden aan dat het nieuwe molecuul inderdaad tegelijkertijd aan twee eiwitpartners kan binden, waardoor het eiwitcomplex tot 40 keer sterker wordt."
Borstkanker
De ontwikkeling van deze "moleculaire lijmen" heeft een groot potentieel voor bepaalde soorten resistente borstkanker. Deze laatste vertonen vaak een overactieve receptor (oestrogeenreceptor α), die momenteel inefficiënt wordt aangevallen via medicijnen die zijn activiteit rechtstreeks proberen te blokkeren. In een recente publicatie, Sijbesma bewees dat het stabiliseren van de interactie van deze receptor met een regulerend eiwit wellicht de beste keuze is. Sijbesma:"Het is bekend dat deze receptor wordt gedownreguleerd door een specifiek eiwit, het hub-eiwit 14-3-3σ. Dus, we hebben moleculaire lijmen ontworpen die de receptor stevig kunnen vasthouden met dit specifieke eiwit en het kunnen inactiveren.
Voorbij kanker
Voor Sijbesma, de centrale innovatie van haar onderzoek is de vaststelling van het onderliggende biologische concept van een moleculaire lijm voor twee eiwitten. Dit zou kunnen leiden tot nieuwe wegen in de ontwikkeling van geneesmiddelen en de behandeling van verschillende ziekten. Sijbesma:"Deze aanpak beperkt zich niet tot toepassingen bij borstkanker, maar het zou in de toekomst nuttig kunnen zijn voor de ontwikkeling van nieuwe therapieën voor ziekten zoals neurodegeneratie, ontsteking, cystische fibrose en diabetes."
 Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik?
Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik? Plant op proefschaal om zeldzame aardelementen te winnen in het hart van het kolenland
Plant op proefschaal om zeldzame aardelementen te winnen in het hart van het kolenland Uitvinding aangewakkerd door COVID-19-pandemie desinfecteert continu veilig oppervlakken
Uitvinding aangewakkerd door COVID-19-pandemie desinfecteert continu veilig oppervlakken Hoe langzamer ze draaien, hoe helderder ze gloeien
Hoe langzamer ze draaien, hoe helderder ze gloeien Middeleeuwse kruitrecepten opblazen
Middeleeuwse kruitrecepten opblazen
Hoofdlijnen
- Wat is er met androgyn gebeurd?
- Het voordeel van het hebben van veel replicatie-origines in een eukaryotisch chromosoom
- Welke organen maken het vaatstelsel op?
- Septate versus niet-Septate Hyphae
- Kun jij een paar haren van een renpaard stelen en je eigen haren klonen?
- Een 3D-model plantencel maken zonder voedsel
- De ongelooflijke reis van de eerste Afrikaanse schildpad die in Europa aankwam
- Wat is Lambda Max?
- Een genetische opstand in het vroege leven voorkomen
- Minuscule moleculaire bewegingen kunnen leiden tot efficiëntere biobrandstofcellen

- Chiraliteit in realtime
- De helix van het leven:nieuwe studie laat zien hoe RNA zich stabiel bindt aan kunstmatige nucleïnezuren
- Complexe moleculen maken in slechts een paar stappen

- Quantum dots houden atomen op afstand om katalyse te stimuleren
 De bizarre sociale geschiedenis van bedden
De bizarre sociale geschiedenis van bedden Hoe de hoeveelheid reagens in Excess
Hoe de hoeveelheid reagens in Excess Hoe word je goed in Math
Hoe word je goed in Math Onderzoek suggereert dat de middelste mantel evenveel water bevat als de oceanen van de aarde
Onderzoek suggereert dat de middelste mantel evenveel water bevat als de oceanen van de aarde Nanobomen oogsten de energie van de zon om water om te zetten in waterstofbrandstof
Nanobomen oogsten de energie van de zon om water om te zetten in waterstofbrandstof Open access sluit wetenschappers uit ontwikkelingslanden uit
Open access sluit wetenschappers uit ontwikkelingslanden uit De groeiende ruimtevaartindustrie worstelt om arbeiders te vinden, maar kan geen buitenlanders aan
De groeiende ruimtevaartindustrie worstelt om arbeiders te vinden, maar kan geen buitenlanders aan Ademhalingscijfers verbeteren met behulp van elektrische velden
Ademhalingscijfers verbeteren met behulp van elektrische velden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com

