
Wetenschap
Wat maken waterstof en koolstof?
Waarom zoveel verbindingen?
* veelzijdige binding: Koolstof heeft vier valentie -elektronen, waardoor het vier bindingen kan vormen met andere atomen, waaronder waterstof. Dit geeft koolstof een opmerkelijk vermogen om lange ketens en complexe structuren te creëren.
* koolwaterstoffen: De eenvoudigste verbindingen gemaakt van alleen waterstof en koolstof worden koolwaterstoffen genoemd. Ze vormen de basis van veel organische moleculen.
Voorbeelden van verbindingen:
* methaan (CH4): De eenvoudigste koolwaterstof, een belangrijke component van aardgas.
* ethaan (C2H6): Nog een eenvoudige koolwaterstof, ook gevonden in aardgas.
* propaan (C3H8): Een veel voorkomende brandstof voor koken en verwarmen.
* Butane (C4H10): Gevonden in lichtere vloeistof en enkele brandstofbronnen.
* ethyleen (C2H4): Een cruciale bouwsteen voor kunststoffen en andere industriële chemicaliën.
* benzeen (C6H6): Een fundamentele verbinding voor veel geneesmiddelen en andere organische chemicaliën.
* polymeren: Lange ketens van herhalende eenheden, waaronder kunststoffen zoals polyethyleen (gemaakt van ethyleen).
voorbij koolwaterstoffen:
Het toevoegen van andere elementen zoals zuurstof, stikstof en zwavel aan de mix creëert nog meer diverse verbindingen. Deze omvatten:
* alcoholen: Bevatten een hydroxylgroep (-oH) zoals ethanol (alcohol drinken).
* aldehydes &ketonen: Heb een carbonylgroep (C =O) zoals aceton (nagellakverwijderaar).
* carbonzuren: Bevatten een carboxylgroep (-cooh) zoals azijnzuur (azijn).
* Amines: Bevatten stikstofachtige methylamine (gebruikt bij de productie van meststof).
Conclusie:
De combinatie van waterstof en koolstof vormt de basis voor een ongelooflijk groot en divers scala aan verbindingen, essentieel voor ons dagelijks leven en de chemie van het leven zelf.
 Kankercellen van patiënten groeien betrouwbaar op nieuwe 3D-steiger, veelbelovend voor precisiegeneeskunde
Kankercellen van patiënten groeien betrouwbaar op nieuwe 3D-steiger, veelbelovend voor precisiegeneeskunde Wat is het beste bewijs voor een chemische reactie?
Wat is het beste bewijs voor een chemische reactie?  Hoe teken je twee isotopen van koolstof en geef je het massanummer voor elk?
Hoe teken je twee isotopen van koolstof en geef je het massanummer voor elk?  Zijn substraat en reactant hetzelfde of anders?
Zijn substraat en reactant hetzelfde of anders?  Hoeveel volle elektronen heeft zwavel?
Hoeveel volle elektronen heeft zwavel?
Hoofdlijnen
- Welke soorten gegevens kunnen in een experiment worden verzameld?
- In welke ecosystemen leeft Meerkat?
- Wat betekent BC en AC in de wetenschap?
- Wat maken wetenschappers om hen een hypothese te helpen en gegevens te verzamelen?
- Welke lagen van de opperhuid verdelen cel?
- Hoe noem je een groep organen die samenwerken om een grote baan te vormen?
- Vissen krimpen als de temperatuur van de oceaan stijgt
- Waarom is de kern erg dicht?
- Studie onderzoekt conflict tussen boeren en roofdieren
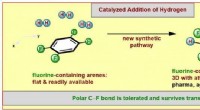
- Een nieuwe methode voor de vorming van gefluoreerde moleculaire ringen
- Onderzoeker creëert chemisch systeem dat vroeg celgedrag nabootst

- In het laboratorium gemaakte eiwit chomps co-factor als een grote ol gator
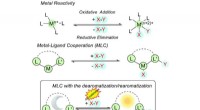
- Aromaatiteit in katalyse begrijpen om nieuwe kansen te ontsluiten
- Aerogel:het microstructuurmateriaal van de toekomst

 Wanneer ontstonden genetische variaties die ons menselijk maken?
Wanneer ontstonden genetische variaties die ons menselijk maken?  Hoe heeft Theodor Schwan bijgedragen aan de celtheorie?
Hoe heeft Theodor Schwan bijgedragen aan de celtheorie?  Wat geeft aan dat er een chemische verandering kan plaatsvinden?
Wat geeft aan dat er een chemische verandering kan plaatsvinden?  Heeft Johannes Kepler planeten ontdekt?
Heeft Johannes Kepler planeten ontdekt?  Ultrakoude polyatomische moleculen maken door ze in drie dimensies te vangen en af te koelen
Ultrakoude polyatomische moleculen maken door ze in drie dimensies te vangen en af te koelen Typen pneumatische systemen
Typen pneumatische systemen  Nieuwe deeltjes rond zwarte gaten detecteren met zwaartekrachtsgolven
Nieuwe deeltjes rond zwarte gaten detecteren met zwaartekrachtsgolven Hybride materiaal brengt transportbrandstofcellen van de volgende generatie dichterbij
Hybride materiaal brengt transportbrandstofcellen van de volgende generatie dichterbij
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

