
Wetenschap
Hoeveel volle elektronen heeft zwavel?
Zwavel heeft 6 Volledige elektronen.
Dit is waarom:
* Elektronenconfiguratie: De elektronenconfiguratie van Sulphur is 1S² 2S² 2P⁶ 3S² 3P⁴.
* Volledige schelpen: De eerste twee elektronenschalen (1S en 2s) zijn volledig gevuld met elk 2 elektronen. De 2P -subshell is ook gevuld met 6 elektronen. Dit betekent dat de eerste twee elektronenschalen (1s, 2s en 2p) volledig vol zijn.
* Gedeeltelijke shell: De 3P -subshell heeft 4 elektronen. Het heeft nog 2 elektronen nodig om volledig te worden gevuld.
Daarom heeft zwavel 6 Volledige elektronen in zijn 1s-, 2s- en 2p -schelpen.
 Chemici hebben de oorsprong van de groene fluorescentie uitgelegd
Chemici hebben de oorsprong van de groene fluorescentie uitgelegd Nieuwe katalysator realiseert ongekende activiteiten
Nieuwe katalysator realiseert ongekende activiteiten Welke van de volgende beschrijft wat er gebeurt als ijzer (Fe) wordt geoxideerd tot Fe2-ionen?
Welke van de volgende beschrijft wat er gebeurt als ijzer (Fe) wordt geoxideerd tot Fe2-ionen?  Microanalyse van biologische monsters voor vroege detectie van ziekten
Microanalyse van biologische monsters voor vroege detectie van ziekten Welke metalen roesten niet?
Welke metalen roesten niet?
 Hoe de risico's van klimaatverandering op nationale schaal toenemen naarmate het niveau van de opwarming van de aarde toeneemt
Hoe de risico's van klimaatverandering op nationale schaal toenemen naarmate het niveau van de opwarming van de aarde toeneemt  Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen
Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen Wat beschrijft de grond het beste in graslanden?
Wat beschrijft de grond het beste in graslanden?  Machine learning voorspelt nieuwe details van geothermische warmtestroom onder de Groenlandse ijskap
Machine learning voorspelt nieuwe details van geothermische warmtestroom onder de Groenlandse ijskap Wat is het verschil tussen wespen en horzels?
Wat is het verschil tussen wespen en horzels?
Hoofdlijnen
- Hoe kan een op coöperaties gebaseerde organisatie van inheemse visserij de veerkracht van afnemende bestanden bevorderen?
- Hoe verbeteren aanpassingen het overleven van een soort?
- Waar is secundaire enzymtekort voort?
- Wat is de vergoeding van natuurlijke hulpbronnen?
- Welk enzym gebruiken wetenschappers om genen uit DNA uit strengen te snijden?
- Prehistorische skeletten van vrouwen tonen impact van rigoureuze handenarbeid
- Wetenschappers ontcijferen mechanismen die ten grondslag liggen aan de biologie van veroudering
- Wat zijn de 3 plantentropismen en hun functies?
- Wat is de algen die een symbiotische relatie hebben met rifbuilders?
- Onderzoekers vinden veelbelovende kandidaten voor nanodeeltjes voor het afvangen en omzetten van koolstofdioxide

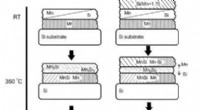
- Natuurkundigen houden toezicht op de vorming van hogere mangaansilicidefilms
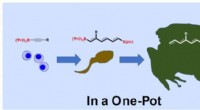
- Nieuwe modellen om de microstructuur van polymeermengsels te onderzoeken

- Tarwegluten kunnen worden gebruikt om duurzaam luiermateriaal te maken

- Onderzoekers ontwikkelen chemische reactiemethode voor efficiëntere medicijnproductie
 Wanneer licht een donker voorwerp raakt, wordt het dan geabsorbeerd?
Wanneer licht een donker voorwerp raakt, wordt het dan geabsorbeerd?  CO2 verminderen met gemeenschappelijke elementen en zonlicht
CO2 verminderen met gemeenschappelijke elementen en zonlicht Waarom verwijdert een blad zuurstof wanneer ondergedompeld in water?
Waarom verwijdert een blad zuurstof wanneer ondergedompeld in water?  Hoe converteer je van gram naar liter met Density
Hoe converteer je van gram naar liter met Density Atomaire imperfecties brengen het kwantumcommunicatienetwerk dichter bij de realiteit
Atomaire imperfecties brengen het kwantumcommunicatienetwerk dichter bij de realiteit Het is moeilijk om iemands valse overtuigingen aan te vechten, omdat hun ideeën afkomstig zijn van sociale netwerken, niet van feiten
Het is moeilijk om iemands valse overtuigingen aan te vechten, omdat hun ideeën afkomstig zijn van sociale netwerken, niet van feiten Cyberbeveiligingstest op ISS
Cyberbeveiligingstest op ISS Magneten zijn chaotisch - en snel - op de allerkleinste schaal
Magneten zijn chaotisch - en snel - op de allerkleinste schaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

