
Wetenschap
Wat zorgt er tijdens de vorming van een verbinding voor dat attracties zich vormen tussen atomen?
Hier is een uitsplitsing van de belangrijkste soorten attracties die betrokken zijn:
* ionische binding: Dit omvat de volledige overdracht van elektronen van het ene atoom naar het andere. Het atoom dat elektronen verliest, wordt een positief geladen ion (kation), terwijl het atoom dat elektronen krijgt een negatief geladen ion (anion) wordt. Deze tegengesteld geladen ionen trekken elkaar vervolgens sterk aan en vormen een ionische binding.
* Covalente binding: Dit omvat het delen van elektronen tussen atomen. De gedeelde elektronen worden aangetrokken tot de positief geladen kernen van beide atomen, waardoor een sterke band tussen hen ontstaat.
* Polaire covalente binding: In dit type covalente binding worden de elektronen niet gelijk gedeeld tussen de atomen. Dit komt omdat het ene atoom een hogere elektronegativiteit heeft (een maat voor zijn vermogen om elektronen aan te trekken) dan het andere. Dit creëert een gedeeltelijke positieve lading op het ene atoom en een gedeeltelijke negatieve lading aan het andere, wat resulteert in een polair molecuul met een dipoolmoment.
* Niet -polaire covalente binding: Wanneer elektronen gelijk worden gedeeld tussen atomen met vergelijkbare elektronegativiteit, ontstaat een niet -polaire covalente binding.
* Metallic binding: In metalen worden de buitenste elektronen losjes vastgehouden door de atomen en kunnen ze vrij door de gehele metalen structuur bewegen. Dit creëert een "zee van elektronen" die de positief geladen metaalionen omringt en ze bij elkaar houdt in een sterke metalen binding.
Samenvattend worden de attracties die zich vormen tussen atomen tijdens samengestelde vorming aangedreven door de fundamentele elektrostatische krachten tussen de positief geladen kernen en negatief geladen elektronen, en het specifieke type aantrekkingskracht hangt af van de aard van de betrokken atomen.
 Wat maakt een gallon calciumchloride -manier?
Wat maakt een gallon calciumchloride -manier?  De sterkte van een zuur en een zuur wordt bepaald door hoe volledig ze dissociëren in water.
De sterkte van een zuur en een zuur wordt bepaald door hoe volledig ze dissociëren in water.  Welk bewijs heb je waargenomen dat zou doen geloven dat het residu kaliumchloride was?
Welk bewijs heb je waargenomen dat zou doen geloven dat het residu kaliumchloride was?  Waarom weerstaat kwarts de chemische verwering meer dan enig ander gemeenschappelijk materiaal?
Waarom weerstaat kwarts de chemische verwering meer dan enig ander gemeenschappelijk materiaal?  Aanpassingen van zeezoogdieren aan een laag zuurstofgehalte bieden een nieuw perspectief op COVID-19
Aanpassingen van zeezoogdieren aan een laag zuurstofgehalte bieden een nieuw perspectief op COVID-19
 Tool ontwikkeld om de voetafdruk van huishoudelijk plastic te berekenen
Tool ontwikkeld om de voetafdruk van huishoudelijk plastic te berekenen Wat is het graslanden klimaat in het voorjaar?
Wat is het graslanden klimaat in het voorjaar?  Filippijnen zetten oproerpolitie in voor sluiting toeristen Boracay
Filippijnen zetten oproerpolitie in voor sluiting toeristen Boracay VS zegt dat lekkende nucleaire afvalkoepel veilig is; Leiders van de Marshalleilanden geloven het niet
VS zegt dat lekkende nucleaire afvalkoepel veilig is; Leiders van de Marshalleilanden geloven het niet Honderden geëvacueerd na instorting dodelijke stortplaats Sri Lanka
Honderden geëvacueerd na instorting dodelijke stortplaats Sri Lanka
Hoofdlijnen
- Deze spitsmuizen hebben koppen die krimpen met het seizoen
- Wetenschappers ontdekken wat een gepantserde dinosaurus at tijdens zijn laatste maaltijd
- Hoe steroïde hormonen planten laten groeien
- Hoe zijn bacteriën nuttig?
- Wat is een voorbeeld van iets dat de basisstructuren een levend organisme mist en homeostase niet kan metaboliseren of onderhouden?
- De voor- en nadelen van mutatie
- Wat gebeurt er met DNA vóór celdeling bij mitose?
- Veranderingen in diervoeder kunnen 1 miljard mensen van voedsel voorzien
- Differentiëren de termen homozygoot en heterozygoot?
- Chemici ontdekken hoe blauw licht blindheid versnelt

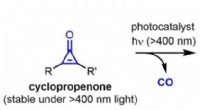
- Fotokatalytische vorming van zeer reactieve alkynen onder zichtbaar licht
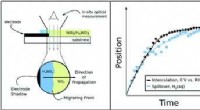
- Hernieuwbare elektriciteit gebruiken voor industriële hydrogeneringsreacties
- Onderzoekers maken van plastic flessenafval ultralicht supermateriaal met brede toepassingen

- Onderzoek zoomt in op enzym dat DNA-schade door UV-stralen herstelt

 Elektrische signalen bepalen optische eigenschappen
Elektrische signalen bepalen optische eigenschappen Door Otago geleid onderzoek om smartphones nog slimmer te maken
Door Otago geleid onderzoek om smartphones nog slimmer te maken Hoeveel centimeters zijn er in 16 inch?
Hoeveel centimeters zijn er in 16 inch?  Welke sterrenbeelden zijn gedurende alle 12 maanden zichtbaar in Bellingham WA?
Welke sterrenbeelden zijn gedurende alle 12 maanden zichtbaar in Bellingham WA?  Welke fossiele brandstofvoorraden moeten in de grond blijven om gevaarlijke klimaatverandering te voorkomen?
Welke fossiele brandstofvoorraden moeten in de grond blijven om gevaarlijke klimaatverandering te voorkomen?  Waarom zijn de oude oceanen van de aarde verdwenen?
Waarom zijn de oude oceanen van de aarde verdwenen? Wat toont een transformatie van chemische naar elektrische en lichte energie?
Wat toont een transformatie van chemische naar elektrische en lichte energie?  Nauwkeuriger lezen van RNA-modificaties in een zakformaatapparaat
Nauwkeuriger lezen van RNA-modificaties in een zakformaatapparaat
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

