
Wetenschap
Wat is meer zure SO2 of SO3?
Dit is waarom:
* Oxidatietoestand: Dus₃ heeft zwavel in een hogere oxidatietoestand (+6) in vergelijking met SO₂ (+4). Hogere oxidatietoestanden leiden in het algemeen tot sterkere zuren.
* Polariteit en bindingssterkte: De zwavel-zuurstofbindingen in SO₃ zijn meer polair en sterker dan die in SO₂. Deze verhoogde polariteit maakt het voor SO₃ gemakkelijker om een proton (H+) te doneren en als een zuur te fungeren.
* stabiliteit van de conjugaatbasis: De geconjugeerde basis van SO₃ (SO₃²⁻) is stabieler dan de geconjugeerde basis van SO₂ (SO₃²⁻). Deze stabiliteit is te wijten aan de delocalisatie van negatieve lading over meerdere zuurstofatomen in SO₃²⁻.
Samenvattend: De hogere oxidatietoestand van zwavel, verhoogde bindingspolariteit en een grotere stabiliteit van de conjugaatbasis in SO₃ dragen allemaal bij aan de hogere zuurgraad in vergelijking met SO₂.
 Onderzoekers realiseren waterstofvorming door contactelektrificatie van watermicrodruppeltjes en de regulering ervan
Onderzoekers realiseren waterstofvorming door contactelektrificatie van watermicrodruppeltjes en de regulering ervan  Hoe werkt PH Paper?
Hoe werkt PH Paper?  Wat zijn gemeenschappelijk gebruik van Xenon?
Wat zijn gemeenschappelijk gebruik van Xenon?  Zelfverdichtend beton wordt duurzamer door gebruik van granietresten
Zelfverdichtend beton wordt duurzamer door gebruik van granietresten Wat zijn de twee ionen die het meest verantwoordelijk zijn voor hard water?
Wat zijn de twee ionen die het meest verantwoordelijk zijn voor hard water?
 De beste manier om klimaatverandering tegen te gaan? Plant een biljoen bomen
De beste manier om klimaatverandering tegen te gaan? Plant een biljoen bomen Wat is de stopste plek op aarde?
Wat is de stopste plek op aarde?  Smog kan FIFA U-17 World Cup uit Delhi dwingen
Smog kan FIFA U-17 World Cup uit Delhi dwingen EPA keert koers over veiligheid van pesticiden die op gewassen worden gebruikt
EPA keert koers over veiligheid van pesticiden die op gewassen worden gebruikt Overstromingen van voedingsstoffen uit meststoffen en afvalwater vervuilen onze rivieren. Zou compenseren kunnen helpen?
Overstromingen van voedingsstoffen uit meststoffen en afvalwater vervuilen onze rivieren. Zou compenseren kunnen helpen?
Hoofdlijnen
- Wat is de onderste lobfunctie?
- Het enige weefsel dat in het lichaam kan contracteren en verkorten?
- Wat is de vrouwelijke gameet?
- Wat is de studie van genomen met of tussen soorten?
- Een plantenceldiagram maken
- Honden die naar de VS worden gebracht, moeten een microchip hebben en ouder zijn dan 6 maanden:CDC
- Wat is wortelcellen functioneren?
- Beschrijf de structuur van nucleotiden en leg uit hoe ze belangrijk zijn voor levende dingen?
- Wat is de cel van een organisme waarvan een virus afhankelijk is?
- Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
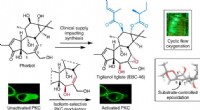
- Enkele nanodeeltjes kunnen de weg vrijmaken voor geneesmiddelen op aanvraag

- Op algen geïnspireerde polymeren verlichten de weg voor verbeterd nachtzicht
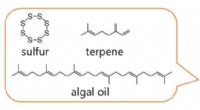
- Gespannen, symmetrisch, en nieuw:tetravinylalleen, een klein maar krachtig molecuul, is voor het eerst gesynthetiseerd
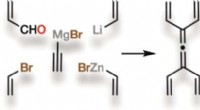
- Nieuwe cyclisatiereacties voor het synthetiseren van macrocyclische medicijnleads

 Onderzoekers identificeren genen die zoogdieren van andere dieren onderscheiden
Onderzoekers identificeren genen die zoogdieren van andere dieren onderscheiden Wetenschappers onderzoeken hoe termieten het paargedrag coördineren voor koloniesucces
Wetenschappers onderzoeken hoe termieten het paargedrag coördineren voor koloniesucces  Hoe kan NY -lichtjaren Hercules zich van de aarde in de war brengen?
Hoe kan NY -lichtjaren Hercules zich van de aarde in de war brengen?  Licht verplaatsen over een halfgeleidende nanodraad via akoestische oppervlaktegolven
Licht verplaatsen over een halfgeleidende nanodraad via akoestische oppervlaktegolven Heeft gas een hoge dichtheid?
Heeft gas een hoge dichtheid?  Hoe de kubieke voet van een cirkel te berekenen
Hoe de kubieke voet van een cirkel te berekenen  Het democratisch bestuur van agrarische multinationals is essentieel voor ecologische duurzaamheid
Het democratisch bestuur van agrarische multinationals is essentieel voor ecologische duurzaamheid Dieren die vlees en planten eten
Dieren die vlees en planten eten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

