
Wetenschap
Hoeveel mol calciumoxide wordt geproduceerd wanneer 36,5 g volledig reageren met zuurstofgas?
1. Schrijf de gebalanceerde chemische vergelijking:
De reactie tussen calcium (Ca) en zuurstof (O₂) produceert calciumoxide (CaO):
2 Ca + O₂ → 2 Cao
2. Bereken de molaire massa calciumoxide (CaO):
* CA:40.08 g/mol
* O:16.00 g/mol
* Cao:40.08 + 16.00 =56.08 g/mol
3. Converteer de massa calcium in mollen:
* Mol ca =(massa van ca) / (molaire massa van ca)
* Mol ca =36,5 g / 40,08 g / mol =0,911 mol
4. Gebruik de molverhouding van de gebalanceerde vergelijking:
De gebalanceerde vergelijking toont aan dat 2 mol Ca reageert om 2 mol CaO te produceren. Dit betekent dat de molverhouding van Ca tot Cao 1:1 is.
5. Bereken de mol calciumoxide geproduceerd:
Aangezien de molverhouding 1:1 is, is het aantal geproduceerde mol CAO gelijk aan het aantal mol CA gereageerd.
* Mol Cao =0,911 mol
Antwoord: 0,911 mol calciumoxide wordt geproduceerd wanneer 36,5 g calcium volledig reageert met zuurstofgas.
 Ontcelde spinazie dient als eetbaar platform voor in het laboratorium gekweekt vlees
Ontcelde spinazie dient als eetbaar platform voor in het laboratorium gekweekt vlees Onderzoek bevordert het begrip van hoe waterstofbrandstof wordt gemaakt
Onderzoek bevordert het begrip van hoe waterstofbrandstof wordt gemaakt  Welke base neutraliseert zwavelzuur?
Welke base neutraliseert zwavelzuur?  Welk molecuul wordt in het Lewis-model als een base beschouwd, maar niet in het Bronsted-Lowry- of Arrhenius-model?
Welk molecuul wordt in het Lewis-model als een base beschouwd, maar niet in het Bronsted-Lowry- of Arrhenius-model?  Wat is de reactie van ijzer en magnesiumsulfaat?
Wat is de reactie van ijzer en magnesiumsulfaat?
 30 miljoen mensen onder hittewaarschuwingen terwijl het westen van de VS broeit
30 miljoen mensen onder hittewaarschuwingen terwijl het westen van de VS broeit Onderzoekers overwinnen uitdagingen om nieuwe tyfoonwaarnemingen te verzamelen
Onderzoekers overwinnen uitdagingen om nieuwe tyfoonwaarnemingen te verzamelen Wat heeft Tree nodig om te overleven?
Wat heeft Tree nodig om te overleven?  Amerikaanse versnellingen voor stijgend dodental bij bosbranden westkust
Amerikaanse versnellingen voor stijgend dodental bij bosbranden westkust Oude rotsen geven aanwijzingen voor de vroege geschiedenis van de aarde
Oude rotsen geven aanwijzingen voor de vroege geschiedenis van de aarde
Hoofdlijnen
- Wat is de wetenschappelijke classificatie van wezelsoorten?
- Wat is een organel dat pakketten wijzigt en materialen uit de cel transporteert?
- Onderzoek onderzoekt de celgebaseerde theorie van bewustzijn en wat deze inhoudt
- Wat is de definitie van voedselweb?
- Het antwoord om elandenpopulaties gezond te houden? Wolven
- Wat betekent het dat de wetenschap zelfcorreceren is?
- Wat maakt gewervelde dieren speciaal? We kunnen leren van lancetten
- Volgens de celtheorie voeren welke structuren basisfuncties van levende wezens uit?
- Voorbeelden van genetische diversiteit
- Nieuwe techniek bouwt superharde metalen uit nanodeeltjes
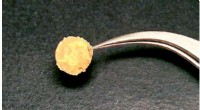
- Uit dikke lucht:kooldioxide omzetten in lichtemitterende koolstof

- Kwantificeren van veranderingen in oppervlaktechemie van houtachtige planten tijdens microbiële fermentatie
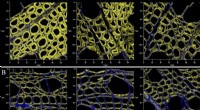
- Gefossiliseerde algen zijn veelbelovend voor verbeterde voedselveiligheidstesten
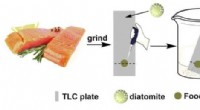
- De gevoeligheid van COVID-tests meten met nieuw materiaal van NIST
 Hoeveel valentie -elektronen heeft een atoom van een halogeen?
Hoeveel valentie -elektronen heeft een atoom van een halogeen?  Hoe worden de aarde opgelijnd tijdens een zonsverduistering?
Hoe worden de aarde opgelijnd tijdens een zonsverduistering?  Uw gewicht op de maan berekenen
Uw gewicht op de maan berekenen  Hoeveel uur duurt het voordat Jupiter rond de zon roteert?
Hoeveel uur duurt het voordat Jupiter rond de zon roteert?  Hubble detecteert beschermend schild dat een paar dwergstelsels verdedigt
Hubble detecteert beschermend schild dat een paar dwergstelsels verdedigt Amerikanen maken zich zorgen over controle over nieuws via sociale media:enquête
Amerikanen maken zich zorgen over controle over nieuws via sociale media:enquête Wat betekent spore-vormende?
Wat betekent spore-vormende?  Wetenschappers ontdekken snellere manier om vasculaire materialen te vervaardigen
Wetenschappers ontdekken snellere manier om vasculaire materialen te vervaardigen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

