
Wetenschap
Wat is het verschil tussen natriumhydroxide en kaliumhydroxide?
1. Chemische formule:
* Natriumhydroxide: Nao
* kaliumhydroxide: Koh
2. Fysieke eigenschappen:
* uiterlijk: Beide zijn witte, geurloze vaste stoffen.
* Oplosbaarheid: Beide zijn zeer oplosbaar in water, waardoor een aanzienlijke hoeveelheid warmte in het proces wordt vrijgegeven (exotherme reactie).
* smeltpunt: NaOH heeft een hoger smeltpunt (318 ° C) dan KOH (360 ° C).
* kookpunt: NaOH heeft een hoger kookpunt (1390 ° C) dan KOH (1324 ° C).
3. Reactiviteit:
* Beide zijn zeer corrosief en kunnen ernstige brandwonden veroorzaken bij contact met huid of ogen.
* Beide reageren gewelddadig met zuren, het vrijgeven van warmte en het vormen van zouten en water.
* KOH wordt over het algemeen als reactiever beschouwd dan NaOH. Dit komt omdat kalium elektropositiever is dan natrium, waardoor de K-OH-binding zwakker en gemakkelijker te breken is.
4. Toepassingen:
* Natriumhydroxide:
* Gebruikt bij de productie van zeep, papier, textiel en wasmiddelen.
* Gebruikt in afvoerreinigers en ovenreinigers vanwege het vermogen om vet en vetten af te breken.
* Gebruikt in de chemische industrie voor verschillende reacties, zoals neutralisatie en hydrolyse.
* kaliumhydroxide:
* Gebruikt bij de productie van vloeibare zepen en shampoos.
* Gebruikt bij de productie van meststoffen en batterijen.
* Gebruikt in de chemische industrie voor verschillende reacties, waaronder de productie van biodiesel en de productie van farmaceutische producten.
Samenvattend zijn de belangrijkste verschillen tussen natriumhydroxide en kaliumhydroxide hun reactiviteit (KOH is meer reactief) en hun specifieke toepassingen.
Het is belangrijk om te onthouden dat zowel natriumhydroxide als kaliumhydroxide gevaarlijke chemicaliën zijn en met extreme voorzichtigheid moeten worden behandeld. Draag altijd geschikte beschermende uitrusting, inclusief handschoenen, bril en een laboratoriumjas, bij het werken met deze stoffen.
Hoofdlijnen
- Studie vindt antimicrobiële resistentie in bodems in heel Schotland
- Wat kunnen haaien ons leren over ons hart?
- Onderzoekers stellen vast hoe supersterk insectenpoten zijn
- Hoe de hersenen van fruitvliegen bepalen wat ze eten
- Wil je de bijen redden? Let op ziekteverwekkers en bloemen
- Wat zijn de gevallen van toevallige ontdekking in de biologie?
- Neemt Aquaporins deel aan actief transport een cel?
- Wat zijn de aanpassingen van een sinaasappelboom?
- Welk type weefsel is ontworpen om voedsel door de spijsverteringsorganen te persen?
- Schelpen en grapefruits inspireren het eerste vervaardigde niet-snijbare materiaal

- Team ontdekt dubbele helixstructuur in synthetisch macromolecuul

- Peptidepapieren wijzen op nieuwe manieren om bacteriën aan te pakken

- Bos- en zeeresten versterken de maag

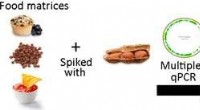
- Op DNA gebaseerde methode detecteert sporen van pinda's in voedingsmiddelen
 Dodental moesson India stijgt tot 159 tientallen nog vermist
Dodental moesson India stijgt tot 159 tientallen nog vermist NASA vindt zware regen in tropische storm Fengshen
NASA vindt zware regen in tropische storm Fengshen Wat zijn golvende functies op sommige zandsteen?
Wat zijn golvende functies op sommige zandsteen?  Een sjabloon voor snelle synthese van nanografenen
Een sjabloon voor snelle synthese van nanografenen Lithium-ionbatterijen tot nieuwe extremen brengen
Lithium-ionbatterijen tot nieuwe extremen brengen Wat is het verschil tussen absolute magnitude en helderheid in termen van het meten van de helderheid van hemellichamen?
Wat is het verschil tussen absolute magnitude en helderheid in termen van het meten van de helderheid van hemellichamen?  Wat voor soort veranderingen smelten en koken?
Wat voor soort veranderingen smelten en koken?  Zetmeel hydrolyseren met warmte en zoutzuur
Zetmeel hydrolyseren met warmte en zoutzuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


