
Wetenschap
Wat is de aantrekkingskracht tussen waterstof- en zuurstofatomen in een waterverbinding?
Dit is waarom:
* polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (nabij de waterstofatomen) en een enigszins negatief uiteinde (nabij het zuurstofatoom).
* Elektrostatische aantrekkingskracht: Het positieve uiteinde van het ene watermolecuul wordt aangetrokken door het negatieve uiteinde van een ander watermolecuul. Deze aantrekkingskracht tussen de enigszins positieve waterstof en de enigszins negatieve zuurstof vormt de waterstofbinding.
Waterstofbindingen zijn zwakker dan covalente bindingen, maar ze zijn sterk genoeg om:
* Houd watermoleculen bij elkaar: Daarom heeft water een relatief hoog kookpunt en oppervlaktespanning.
* beïnvloed de eigenschappen van veel biologische moleculen: Waterstofbindingen spelen een cruciale rol in de structuur en functie van eiwitten, DNA en andere belangrijke moleculen.
 Hoe verklaart u deze feiten N-butylalcohol heeft een veel hoger kookpunt dan zijn isomeer-ethylether, maar beide verbindingen hebben dezelfde oplosbaarheid in water?
Hoe verklaart u deze feiten N-butylalcohol heeft een veel hoger kookpunt dan zijn isomeer-ethylether, maar beide verbindingen hebben dezelfde oplosbaarheid in water?  Een onderzoek naar katalysatoren voor het synthetiseren van polyethyleen met ultrahoog molecuulgewicht
Een onderzoek naar katalysatoren voor het synthetiseren van polyethyleen met ultrahoog molecuulgewicht Illinois-onderzoekers theorie van transport op porieschaal om verbeterde stroombatterijen mogelijk te maken
Illinois-onderzoekers theorie van transport op porieschaal om verbeterde stroombatterijen mogelijk te maken Waarom naftalene sublimes bij kamertemperatuur als het smeltpunt 80 graden is?
Waarom naftalene sublimes bij kamertemperatuur als het smeltpunt 80 graden is?  Wat is de elektronenconfiguratie voor CI?
Wat is de elektronenconfiguratie voor CI?
 Hoe zich te ontdoen van mieren op zoek naar water
Hoe zich te ontdoen van mieren op zoek naar water  Onderzoekers brengen in kaart hoe aanpassingsstrategieën voor de stijging van de zeespiegel de economieën en overstromingen beïnvloeden
Onderzoekers brengen in kaart hoe aanpassingsstrategieën voor de stijging van de zeespiegel de economieën en overstromingen beïnvloeden  Wat zijn de vijf landen in een gematigde zone?
Wat zijn de vijf landen in een gematigde zone?  Wat is de variabele van het wetenschapsbeursproject Apple Mummy?
Wat is de variabele van het wetenschapsbeursproject Apple Mummy?  Cyprus worstelt met afvalbeheer nu het aantal toeristen stijgt
Cyprus worstelt met afvalbeheer nu het aantal toeristen stijgt
Hoofdlijnen
- Hoe kunnen we het gebruik van pesticiden terugdringen en boeren tegelijk empoweren? Een genuanceerder aanpak zou kunnen helpen
- Wat is de wetenschappelijke term voor iets dat geen organisme?
- De kanalen die natrium en kalium in het axon transporteren, worden genoemd?
- Wat kunnen fossiele schelpdieren ons vertellen over onze ecologische toekomst? Veel.
- Als u een adenine vindt op een sporten DNA met welke basis wordt deze verbonden?
- Variatie bestaat binnen de genen van elke populatie of soort als resultaat Wat?
- Is een scavenger autotrofe of heterotrofe?
- Onderzoeken hoe microbiomen onze gezondheid beïnvloeden
- De uitgebreide kreten om voedsel van zangvogels vertonen de eerste tekenen van stemonderwijs
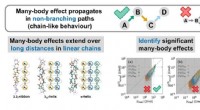
- Wanneer zijn veellichaamseffecten significant?
- Microdeeltjes gecreëerd door een nieuwe 3D-fabricagemethode kunnen lang na injectie medicijnen of vaccins vrijgeven

- Chemici veranderen de richting van de Diels-Alder-reactie volledig

- Omzetting van CO2 naar CO op kamertemperatuur:een nieuwe manier om koolwaterstoffen te synthetiseren

- Noodzaak van rigoureuze procedures binnen de elektrochemische productie van ammoniak

 Mold & Cast Fossils
Mold & Cast Fossils Seks? Het begon allemaal 385 miljoen jaar geleden (met video)
Seks? Het begon allemaal 385 miljoen jaar geleden (met video)  Nieuwe katalysator geeft een boost aan de volgende generatie EV-batterijen
Nieuwe katalysator geeft een boost aan de volgende generatie EV-batterijen Welke soorten rotsen zijn te vinden in Australië?
Welke soorten rotsen zijn te vinden in Australië?  Kan Philly een broeikas voor bananen en ananas worden als het klimaat warmer wordt?
Kan Philly een broeikas voor bananen en ananas worden als het klimaat warmer wordt?  Hoe mensen het ecosysteem ontwrichten
Hoe mensen het ecosysteem ontwrichten  Geen demontage vereist:niet-destructieve methode om de levensduur van dragers in SiC . te meten
Geen demontage vereist:niet-destructieve methode om de levensduur van dragers in SiC . te meten NASA ziet tropische storm Irwin bewegen in de post-tropische storm Hilarys kielzog
NASA ziet tropische storm Irwin bewegen in de post-tropische storm Hilarys kielzog
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

