
Wetenschap
Hoeveel aantal enige paren -elektronen zijn er in chloor?
Chloor heeft drie Eenzame paar elektronen.
Dit is waarom:
* de elektronische configuratie van chloor: Chloor heeft 17 elektronen, met de configuratie:1S² 2S² 2P⁶ 3S² 3P⁵
* valentie -elektronen: De buitenste schaal (3S² 3P⁵) heeft 7 elektronen, wat betekent dat chloor nog een nodig heeft om een stabiel octet te bereiken.
* binding: Chloor vormt meestal één covalente binding en deelt een elektron met een ander atoom. Dit laat 6 elektronen achter in zijn buitenste schaal.
* eenzame paren: Deze 6 elektronen zijn gerangschikt in drie paren, die alleenstaande paren worden genoemd.
Daarom heeft chloor drie Eenzame paar elektronen.
 Welke rol spelen planten in de watercyclus?
Welke rol spelen planten in de watercyclus?  Het scheepsverkeer daalde tijdens de eerste maanden van de COVID-pandemie
Het scheepsverkeer daalde tijdens de eerste maanden van de COVID-pandemie Negen dingen waar je van houdt die worden verwoest door klimaatverandering
Negen dingen waar je van houdt die worden verwoest door klimaatverandering Nieuw onderzoek identificeert dodelijk verborgen weersgevaar dat miljoenen mensen kan treffen
Nieuw onderzoek identificeert dodelijk verborgen weersgevaar dat miljoenen mensen kan treffen Is een ecosysteem de grootste eenheid van ecologische metingen?
Is een ecosysteem de grootste eenheid van ecologische metingen?
Hoofdlijnen
- Verrassende ontdekking - hoe de Afrikaanse tseetseevlieg echt je bloed drinkt
- Faagresistente E. coli-stammen ontwikkeld om mislukte fermentatie te verminderen
- Hoe chimere, druppelvormende eiwitten kunnen bijdragen aan kanker
- Wat doet het enzymcoagulase?
- Selenium beschermt specifieke interneuronen in de hersenen
- In welke cel komt ademhaling op?
- Nieuw onderzoek naar spermastamcellen heeft gevolgen voor mannelijke onvruchtbaarheid en kanker
- Hoe verbeteren aanpassingen het overleven van een soort?
- De genen van kinderen beïnvloeden hoe goed zij profiteren van onderwijs
- Een toekomst van behulpzame engineered living machines?

- Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie

- Katalytische protocellen worden zingy

- Meer edele metalen recyclen uit nucleair en elektronisch afval met behulp van het Picasso-pigment, Pruisisch blauw

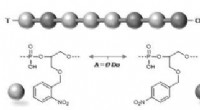
- Geheime berichten verborgen in lichtgevoelige polymeren
 Welk golflengtebereik in het elektromagnetische spectrum is het meest bruikbaar gebleken onderzoek naar stergeboorte dichte moleculaire wolken?
Welk golflengtebereik in het elektromagnetische spectrum is het meest bruikbaar gebleken onderzoek naar stergeboorte dichte moleculaire wolken?  Als een netto koppel wordt toegepast op een object dat zal ervaren welke van de volgende constante hoeksnelheidsversnelling of toenemende traagheidsmoment?
Als een netto koppel wordt toegepast op een object dat zal ervaren welke van de volgende constante hoeksnelheidsversnelling of toenemende traagheidsmoment?  De sterke krachten zijn alleen krachtig als neutronen en protonen zijn?
De sterke krachten zijn alleen krachtig als neutronen en protonen zijn?  Hoe is het Pauli -uitsluitingsprincipe van toepassing op gedrag van deeltjes in de buurt van gebeurtenishorizon zwarte gaten?
Hoe is het Pauli -uitsluitingsprincipe van toepassing op gedrag van deeltjes in de buurt van gebeurtenishorizon zwarte gaten?  Zonder deze uitvinding zouden mensen nooit bij de maan zijn gekomen?
Zonder deze uitvinding zouden mensen nooit bij de maan zijn gekomen?  Great Southern Reef verliest enorm leefgebied voor zeewier door opwarming van de oceaan
Great Southern Reef verliest enorm leefgebied voor zeewier door opwarming van de oceaan Cryo-EM-beelden met hoge resolutie uit Afrika effenen de weg naar op maat gemaakte nitrilasen voor de industrie
Cryo-EM-beelden met hoge resolutie uit Afrika effenen de weg naar op maat gemaakte nitrilasen voor de industrie Als je de creatie van tektonische platen wilt traceren met behulp van magnetische banden normaal en omgekeerde polariteit, zouden je beste plaats maatstrepen zijn?
Als je de creatie van tektonische platen wilt traceren met behulp van magnetische banden normaal en omgekeerde polariteit, zouden je beste plaats maatstrepen zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

