
Wetenschap
Waarom wordt zilveren chloride grijs in zonlicht?
Hier is de uitsplitsing:
* Sunlight's Energy: Zonlicht bevat ultraviolette (UV) straling, die voldoende energie draagt om de chemische binding tussen zilver en chloor in zilverchloride te doorbreken.
* Ontleding: Wanneer AGCL UV-licht absorbeert, zorgt de energie ervoor dat de chloride-ionen (Cl-) worden vrijgegeven als chloorgas (CL2), waardoor zilvermetaal (Ag) achterblijft.
* kleurverandering: Zilvermetaal is grijs van kleur, wat resulteert in de waargenomen grijze verkleuring van het zilveren chloride.
De reactie kan worden weergegeven door de volgende vergelijking:
2agcl (s) → 2ag (s) + cl2 (g)
Factoren die de verkleuringssnelheid beïnvloeden:
* intensiteit van zonlicht: Sterkere UV -straling leidt tot snellere ontleding.
* Aanwezigheid van onzuiverheden: Sommige onzuiverheden kunnen als katalysatoren fungeren en het proces versnellen.
* Temperatuur: Hogere temperaturen versnellen in het algemeen de chemische reacties.
Opmerking: Daarom wordt zilverchloride gebruikt in fotografie. De lichtgevoelige kristallen worden blootgesteld aan licht, wat de ontleding van zilverchloride veroorzaakt. De hoeveelheid licht die elk deel van de film raakt, bepaalt de hoeveelheid gevormde zilvermetaal, wat resulteert in een fotografisch beeld.
 Het naderen van een ideale aminozuursynthese met behulp van waterstof
Het naderen van een ideale aminozuursynthese met behulp van waterstof Wanneer u de pH verlaagt van een oplossing die waterig natriumbenzoaat -neerslag bevat, vormt uiteindelijk wat er zal gebeuren als u na reactie wordt verhoogd door NaOH toe te voegen?
Wanneer u de pH verlaagt van een oplossing die waterig natriumbenzoaat -neerslag bevat, vormt uiteindelijk wat er zal gebeuren als u na reactie wordt verhoogd door NaOH toe te voegen?  Zit er nikkel in wasmiddel?
Zit er nikkel in wasmiddel?  Nanopore-technologie met DNA-computing detecteert gemakkelijk microRNA-patronen van longkanker
Nanopore-technologie met DNA-computing detecteert gemakkelijk microRNA-patronen van longkanker Wat zijn enkele van de factoren die bijdragen aan de CO2-uitstoot in de atmosfeer?
Wat zijn enkele van de factoren die bijdragen aan de CO2-uitstoot in de atmosfeer?
 Wetenschappers bereiden zich voor op expeditie van een jaar naar Arctisch centrum
Wetenschappers bereiden zich voor op expeditie van een jaar naar Arctisch centrum IJskapstudie belooft nieuwe vooruitzichten voor nauwkeurige lokale klimaatprojecties internationaal
IJskapstudie belooft nieuwe vooruitzichten voor nauwkeurige lokale klimaatprojecties internationaal Afbeelding:Sagaing Division in het noordwesten van Myanmar
Afbeelding:Sagaing Division in het noordwesten van Myanmar Wat is de droogste plek op aarde?
Wat is de droogste plek op aarde?  Een natuurlijke kracht van aantrekkingskracht die door de aarde wordt uitgeoefend op objecten die naar het midden trekt, wordt wat genoemd?
Een natuurlijke kracht van aantrekkingskracht die door de aarde wordt uitgeoefend op objecten die naar het midden trekt, wordt wat genoemd?
Hoofdlijnen
- Verschillen langlevende gewassen van jaarlijkse gewassen in hun genetische reactie op menselijke domesticatie?
- Heeft celmembraan zowel dier- als plantencellen?
- Tijdens glycolyse wordt ATP geproduceerd hoeveel netto moleculen worden gevormd?
- Biomedical Engineering Project Onderwerpen voor High School
- Wat zijn de belangrijkste wetenschapsvelden?
- Wat is een endotherme reactie?
- Tot welke groep behoren vitamines?
- Wat zijn enkele overeenkomsten tussen fenotype en genotype?
- Vonnis voor natuurmysterie in Nevada, waar uit DNA-tests blijkt dat wolven coyotes waren
- Nieuw, op waterbasis, recyclebare membraanfilters alle soorten nanodeeltjes
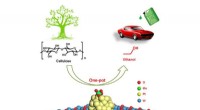
- Wetenschappers ontwikkelen een chemokatalytische benadering voor een-potreactie van cellulose-ethanol
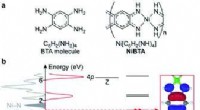
- Onderzoekers systematiseren de methoden voor de synthese van azocine-bevattende systemen

- Koolstofopname neemt de vorm aan van een spons met een nieuwe, kosteneffectieve methode
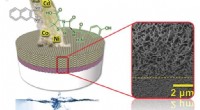
- Wetenschappers ontrafelen de werkingsprincipes van een veelbelovend materiaal voor het snel opladen van batterijen
 Welke factor kan de voortdurende verandering in een ecosysteem beïnvloeden. Verdere verstoringen of langdurige klimaatveranderingen introductie van nonavtie-soorten?
Welke factor kan de voortdurende verandering in een ecosysteem beïnvloeden. Verdere verstoringen of langdurige klimaatveranderingen introductie van nonavtie-soorten?  Het risico op botsingen met ruimteschroot verminderen
Het risico op botsingen met ruimteschroot verminderen Welke substantie in zeewater dat uit de atmosfeer komt?
Welke substantie in zeewater dat uit de atmosfeer komt?  Japan maakt krater op asteroïde om ondergrondse monsters te krijgen
Japan maakt krater op asteroïde om ondergrondse monsters te krijgen Relatie tussen natuurkunde en informatietechnologie?
Relatie tussen natuurkunde en informatietechnologie?  Welke elementen zijn aanwezig in de volgende verbinding Ki?
Welke elementen zijn aanwezig in de volgende verbinding Ki?  Hack-a-vote:Studenten leren hoe kwetsbaar elektronisch stemmen werkelijk is
Hack-a-vote:Studenten leren hoe kwetsbaar elektronisch stemmen werkelijk is  Hoe kunnen we de kinetische energie van een massa van vijf kg vergroten net voordat deze mes raakt?
Hoe kunnen we de kinetische energie van een massa van vijf kg vergroten net voordat deze mes raakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

