
Wetenschap
Wanneer u de pH verlaagt van een oplossing die waterig natriumbenzoaat -neerslag bevat, vormt uiteindelijk wat er zal gebeuren als u na reactie wordt verhoogd door NaOH toe te voegen?
1. Het verlagen van de pH:
* reactie: Wanneer u de pH verlaagt van een oplossing die natriumbenzoaat bevat (NAC 7 H 5 O 2 ), je voegt in wezen zuur toe (H
+
). Dit zuur reageert met het benzoaatanion (C 7 H 5 O 2
`` `
C 7 H 5 O 2
`` `
* neerslag: Benzoëzuur is een zwak zuur en is minder oplosbaar in water dan zijn zoutvorm, natriumbenzoaat. Naarmate de concentratie van benzoëzuur toeneemt, bereikt het zijn oplosbaarheidslimiet en neerslaat uit oplossing als een witte vaste stof.
2. De pH verhogen:
* reactie: Het toevoegen van NaOH aan de oplossing verhoogt de pH (maakt deze eenvoudiger). De hydroxide-ionen (oh
-
) van NaOh reageren met het benzoëzuur, het omzetten van het terug naar benzoaationen:
`` `
C 7 H 6 O 2 (aq) + oh
-
(aq) ⇌ c 7 H 5 O 2
`` `
* ontbinding: Naarmate de concentratie van benzoaationen toeneemt, zal het neerslag van benzoëzuur oplossen. Dit komt omdat het evenwicht terug verschuift naar de vorming van de meer oplosbare benzoaationen.
Samenvattend:
Door de pH te verlagen, creëert u een omgeving die de vorming van benzoëzuur bevordert, wat leidt tot neerslag. Door de pH opnieuw te verhogen, verplaatst u het evenwicht terug naar de vorming van benzoaationen, waardoor het neerslag oplost.
 Wanneer ontstaat er een polaire binding?
Wanneer ontstaat er een polaire binding?  Hoe crack-cocaïne werkt
Hoe crack-cocaïne werkt  Waarom papieren op zichzelf gemakkelijk in brand vat, terwijl een stuk rond een aluminium pijp dat niet doet?
Waarom papieren op zichzelf gemakkelijk in brand vat, terwijl een stuk rond een aluminium pijp dat niet doet?  Dodelijke medicijnen? Wetenschappers werpen licht op het duistere geheim van de flacon van koningin Hatsjepsoet
Dodelijke medicijnen? Wetenschappers werpen licht op het duistere geheim van de flacon van koningin Hatsjepsoet  Wat is de functie van zonlicht in tests van broomwater en jodiumoplossing?
Wat is de functie van zonlicht in tests van broomwater en jodiumoplossing?
 Waarom is Portugal zo gevoelig voor bosbranden?
Waarom is Portugal zo gevoelig voor bosbranden? Oceaanmicroben kunnen interageren met vervuiling om het klimaat te beïnvloeden
Oceaanmicroben kunnen interageren met vervuiling om het klimaat te beïnvloeden Het pleidooi voor het delen van het risico op koolstofopslag
Het pleidooi voor het delen van het risico op koolstofopslag  Chronische dysenterie was waarschijnlijk niet de moordenaar van Edward Black Prince, ondanks wat algemeen wordt aangenomen
Chronische dysenterie was waarschijnlijk niet de moordenaar van Edward Black Prince, ondanks wat algemeen wordt aangenomen  Een soort die een Envirmoent binnenkomt waar het nog niet eerder heeft gewoond, wordt een genoemd?
Een soort die een Envirmoent binnenkomt waar het nog niet eerder heeft gewoond, wordt een genoemd?
Hoofdlijnen
- Het beperkte aanpassingsvermogen maakt zoetwaterbacteriën kwetsbaar voor klimaatverandering
- Waarom wordt het vervuilingsniveau gemeten als aantal kolonies in plaats van kolonies in de grootte?
- Vluchtpatronen onthullen hoe muggen gastheren vinden om dodelijke ziekten over te brengen
- Heeft de gezondheidsstatus van de vader bij muggen invloed op de resultaten van de nakomelingen van de moeder?
- Leg uit waarom het term vloeibare mozaïekmodel wordt gebruikt om het plasmamembraan te beschrijven?
- Hoe speelt osmose een rol bij wat cellen binnenkomt en verlaat?
- Waar bestaan algemene sense -organen uit?
- Wat zijn de letters voor blauwe ogen als het gaat over genetica?
- Welke structuur in een cel bestaat voornamelijk uit fosfolipide dubbellaag?
- Nieuw type binnenzonnecellen voor slimme verbonden apparaten

- Lichtgewicht metalen schuimblokken blastwave, puin van explosieve granaten

- Radiale synthese is baanbrekend voor chemisch onderzoek en productie

- Onderzoekers creëren kunstmatige organellen om cellulair gedrag te controleren
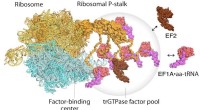
- High-speed atomic force microscopie visualiseert celeiwitfabrieken
 Burgerwetenschappers ontdekken zeldzame kosmische koppeling
Burgerwetenschappers ontdekken zeldzame kosmische koppeling Nieuwe fotokatalysator versnelt de omzetting van kooldioxide in chemische hulpbronnen
Nieuwe fotokatalysator versnelt de omzetting van kooldioxide in chemische hulpbronnen Wat zijn de ribosomen van een mobiele telefoon?
Wat zijn de ribosomen van een mobiele telefoon?  Everyday Mathematics Vs. Singapore Mathematics
Everyday Mathematics Vs. Singapore Mathematics Wat zijn de voordelen van protisten?
Wat zijn de voordelen van protisten?  Welke oplossingen hebben een groter aantal hydroxide -ionen dan waterstofionen?
Welke oplossingen hebben een groter aantal hydroxide -ionen dan waterstofionen?  Naarmate bosbranden erger worden, rook verspreidt zich, wekt gezondheidsproblemen op
Naarmate bosbranden erger worden, rook verspreidt zich, wekt gezondheidsproblemen op Wat is de climax in Where Mountain Meets Moon?
Wat is de climax in Where Mountain Meets Moon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

