
Wetenschap
Wat is het verschil tussen hydroxide- en oxide -proerten?
hydroxiden
* chemische formule: Bevat het hydroxide -ion (OH⁻).
* Natuur: Gewoonlijk ionische verbindingen, wat betekent dat ze worden gevormd door de elektrostatische aantrekkingskracht tussen een positief geladen metaalion en een negatief geladen hydroxide -ion.
* eigenschappen:
* basiciteit: Hydroxiden zijn over het algemeen basic (alkalisch), wat betekent dat ze reageren met zuren om zouten en water te vormen.
* Oplosbaarheid: De oplosbaarheid varieert sterk, afhankelijk van het betrokken metaal. Sommige hydroxiden zijn zeer oplosbaar (bijv. NaOH, KOH), terwijl anderen praktisch onoplosbaar zijn (bijv. Fe (OH) ₃, Cu (OH) ₂).
* Reactiviteit: Hydroxiden kunnen reageren met zuren, sommige reageren met water en sommige kunnen ontleden bij de verwarming.
* Voorbeelden: Natriumhydroxide (NaOH), kaliumhydroxide (KOH), calciumhydroxide (Ca (OH) ₂), aluminiumhydroxide (AL (OH) ₃).
oxiden
* chemische formule: Bevat het oxide -ion (o²⁻).
* Natuur: Kan ionisch, covalent of een combinatie van beide zijn.
* eigenschappen:
* Acidity/Basicity: De zuurgraad of basiciteit van een oxide hangt af van het metaal of niet-metaal waarmee het wordt gecombineerd.
* Basisoxiden: Typisch gevormd door metalen en reageren met water om hydroxiden te vormen. Ze reageren ook met zuren om zouten en water te vormen. (bijv. Na₂o, Cao)
* zure oxiden: Typisch gevormd door niet-metalen en reageren met water om zuren te vormen. Ze reageren ook met bases om zouten en water te vormen. (bijv. So₂, co₂)
* amfoterische oxiden: Deze oxiden kunnen zich gedragen als zowel zuren als basen. Ze reageren met zowel zuren als basen. (bijv. Al₂o₃, Zno)
* Oplosbaarheid: Oplosbaarheid varieert sterk. Sommige oxiden zijn oplosbaar in water, terwijl andere onoplosbaar zijn.
* Reactiviteit: Oxiden kunnen reageren met zuren, basen, water en andere oxiden.
* Voorbeelden: Natriumoxide (Na₂o), kooldioxide (CO₂), ijzeroxide (Fe₂o₃), siliciumdioxide (SIO₂).
Sleutelverschillen
* anion: Hydroxiden bevatten het hydroxide -ion (OH⁻), terwijl oxiden het oxide -ion bevatten (o²⁻).
* basiciteit: Hydroxiden zijn typisch eenvoudig, terwijl oxiden basic, zuur of amfoterisch kunnen zijn, afhankelijk van het betrokken element.
* Formatie: Hydroxiden worden vaak gevormd door de reactie van een metaaloxide met water, terwijl oxiden kunnen worden gevormd door verschillende reacties.
Samenvattend:
Zie hydroxiden als "gehydrateerde" oxiden. Ze hebben het extra waterstofatoom in vergelijking met oxiden. Dit extra waterstofatoom is wat hydroxiden hun verschillende chemische eigenschappen geeft.
 Oneindig recyclebaar polymeer toont praktische eigenschappen van kunststoffen
Oneindig recyclebaar polymeer toont praktische eigenschappen van kunststoffen Wie is werk dat het meest heeft bijgedragen aan het model van een atoom?
Wie is werk dat het meest heeft bijgedragen aan het model van een atoom?  Ontwerpmateriaal om plastic buiten de vuilstort te houden
Ontwerpmateriaal om plastic buiten de vuilstort te houden Wat is de eenvoudigste formule voor verbinding gevormd tussen fosfor en overtollig chloor?
Wat is de eenvoudigste formule voor verbinding gevormd tussen fosfor en overtollig chloor?  Is natriumchloride polair of niet, je bent in de war omdat sommigen zeggen dat het en polair is?
Is natriumchloride polair of niet, je bent in de war omdat sommigen zeggen dat het en polair is?
 Het opruimen van giftige sites mag de buren niet opruimen
Het opruimen van giftige sites mag de buren niet opruimen Nieuw onderzoek onthult dat Britse eilanden 2,5 miljoen jaar geleden onder ijskappen werden begraven
Nieuw onderzoek onthult dat Britse eilanden 2,5 miljoen jaar geleden onder ijskappen werden begraven Welke wetenschapper gaf wetten van reflectie?
Welke wetenschapper gaf wetten van reflectie?  Palmolie niet de enige oorzaak van bosverlies in Indonesië
Palmolie niet de enige oorzaak van bosverlies in Indonesië De Grote Groene Muur van Afrika is een natuurbehoud - en wereldwonder
De Grote Groene Muur van Afrika is een natuurbehoud - en wereldwonder
Hoofdlijnen
- Wat zijn twee soorten organismen in de stikstoffixatie?
- Wat is het voedselproducerende proces in planten?
- Wat is beschrijvingonderzoek?
- Wetenschappers ontdekken een nieuw mechanisme voor de export van bacteriële polysachariden
- Is Verrucomicrobia een slechte of goede bacteriën?
- De hectische 24-uurs inspanning om een bedreigde, verweesde vleermuis
- Hoe dragen dieren zoals het afgebeelde hert bij aan de stikstofcyclus?
- Hoe gedraag je je in een dierentuin - volgens de wetenschap
- Wat is dierenwetenschap en technologie?
- Forensische wetenschappers ontsluiten unieke chemische handtekeningen in banden

- Onderzoekers maken slim staal, 30% sterker

- Onderzoekers kunnen rekenen op verbeterde proteomics-methode

- Polymeren bundelen hun krachten om te leveren

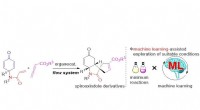
- Lastige reactiereeks krijgt een grote boost van een stroomopstelling en statistieken
 Mexico verhoogt bescherming op pre-Spaanse ceremoniële site
Mexico verhoogt bescherming op pre-Spaanse ceremoniële site  Waar vind je de hoogste berg op het zonnestelsel?
Waar vind je de hoogste berg op het zonnestelsel?  Hoe vaak kun je 's nachts een maan zien?
Hoe vaak kun je 's nachts een maan zien?  Hoeveel energie produceert een grote windturbine?
Hoeveel energie produceert een grote windturbine?  Hubble bekijkt kosmische stofbanen
Hubble bekijkt kosmische stofbanen  Wat is het ontstaan van kleur?
Wat is het ontstaan van kleur?  Hoe een vis kan braden:wetenschappers ontdekken evolutionaire aanwijzingen achter elektriciteit
Hoe een vis kan braden:wetenschappers ontdekken evolutionaire aanwijzingen achter elektriciteit  Grafeenfilter maakt koolstofafvang efficiënter en goedkoper
Grafeenfilter maakt koolstofafvang efficiënter en goedkoper
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

