
Wetenschap
Wat is het aantal moleculen in 16,75 gram H2O?
1. Vind de molaire watermassa:
* H₂o heeft twee waterstofatomen (elk 1,01 g/mol) en één zuurstofatoom (16,00 g/mol).
* Molaire massa van H₂o =(2 * 1.01 g/mol) + (16.00 g/mol) =18,02 g/mol
2. Converteer grams naar mollen:
* mol =massa / molaire massa
* Moles =16,75 g / 18.02 g / mol
* mol ≈ 0,93 mol
3. Gebruik het nummer van Avogadro:
* Het nummer van Avogadro stelt dat er 6.022 x 10²³ moleculen in één mol van elke stof zijn.
* Aantal moleculen =mollen * Avogadro's nummer
* Aantal moleculen ≈ 0,93 mol * 6.022 x 10²³ Moleculen/mol
* Aantal moleculen ≈ 5,60 x 10²³ Moleculen
Daarom zijn er ongeveer 5,60 x 10²³ moleculen in 16,75 gram water.
 Abrupte dooi van de permafrost blijkt de opwarmingseffecten op de CO₂-uitstoot in de bodem te versterken
Abrupte dooi van de permafrost blijkt de opwarmingseffecten op de CO₂-uitstoot in de bodem te versterken  Geheimen van verborgen ijscanyons onthuld
Geheimen van verborgen ijscanyons onthuld Afbeelding:Siberische bosbranden gezien vanuit een baan om de aarde
Afbeelding:Siberische bosbranden gezien vanuit een baan om de aarde Bescherming voor volle zee is cruciaal om kwetsbare kustgemeenschappen te beschermen - nieuw onderzoek
Bescherming voor volle zee is cruciaal om kwetsbare kustgemeenschappen te beschermen - nieuw onderzoek Ontdekking van hoge aardwarmte op Zuidpool
Ontdekking van hoge aardwarmte op Zuidpool
Hoofdlijnen
- Wetenschappers ontwikkelen nieuwe techniek om vlees te kweken in het laboratorium met behulp van magnetisch veld
- Welke soorten wereldwijde veranderingen betreffen biologen?
- Waarom blijft een cel even groot in een isotone oplossing?
- Zuid-Korea gaat de berenhouderij verbieden, maar wat te doen met de honderden in gevangenschap levende dieren die nog overblijven?
- Wat zijn plantensystemen?
- Welke delen van de cel kun je onder een microscoop* zien?
- NOAA rapporteert een aanhoudende daling van de overbevissing
- Kunnen eiwitten afzonderlijke domeinen hebben met verschillende structuren en functies?
- De wilde ezel keert terug
- Een effectieve manier om atrazin en zijn bijproducten in oppervlaktewater te elimineren

- Door dik en dun:neutronen volgen lithiumionen in batterij-elektroden

- Eenkristallen diamant klaar maken voor elektronica
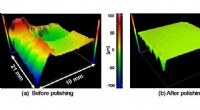
- Onderzoekers onderzoeken structurele veranderingen in snel ingevroren eiwitten
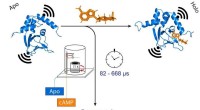
- Antilichaam tegen kankerverwekkende stof ontcijferd

 Wat is de golflengte van een golf met snelheid 345 ms en frequentie 600 Hz?
Wat is de golflengte van een golf met snelheid 345 ms en frequentie 600 Hz?  3Q's:Waarom gevangenissen met winstoogmerk in opkomst zijn
3Q's:Waarom gevangenissen met winstoogmerk in opkomst zijn  Honingbijen stemmen om te beslissen over nestplaatsen – waarom we zouden moeten luisteren
Honingbijen stemmen om te beslissen over nestplaatsen – waarom we zouden moeten luisteren  Rocket Balloon Races, Two Ways
Rocket Balloon Races, Two Ways Wat is een kracht die de beweging behoudt?
Wat is een kracht die de beweging behoudt?  Wat is de landvorm van Halifax?
Wat is de landvorm van Halifax?  Waarvoor wordt boorzuur gebruikt?
Waarvoor wordt boorzuur gebruikt?  Bedrijfspartnerschappen kunnen interne gevolgen hebben
Bedrijfspartnerschappen kunnen interne gevolgen hebben
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

