
Wetenschap
Wat is de moleculaire vorm van C2H5CL?
Dit is waarom:
* centraal atoom: Het centrale atoom in C2H5CL is het koolstofatoom dat is gebonden aan het chlooratoom.
* Hybridisatie: Dit koolstofatoom heeft vier elektronendomeinen (één enkele binding aan het chlooratoom, de ene enkele binding aan het andere koolstofatoom en twee enkele bindingen aan waterstofatomen). Dit betekent dat het SP3 -hybridisatie ondergaat.
* Vorm: SP3 -hybridisatie resulteert in een tetraëdrische geometrie, wat betekent dat het centrale koolstofatoom zich in het midden van een tetraëder bevindt met zijn vier bindingen die naar de hoeken wijzen.
Opmerking: Hoewel het totale molecuul niet strikt tetraëdrisch is vanwege de aanwezigheid van het andere koolstofatoom, vertoont de koolstof direct bond aan chloor tetraëdrische geometrie eromheen.
 Bedrijven sleutel tot het redden van de natuur, zegt WWF-chef
Bedrijven sleutel tot het redden van de natuur, zegt WWF-chef Orkaan Isaias raast aan wal aan Amerikaanse oostkust
Orkaan Isaias raast aan wal aan Amerikaanse oostkust Wat is een element in de wetenschap en een voorbeeld geven?
Wat is een element in de wetenschap en een voorbeeld geven?  Studie vindt de vingerafdruk van padie in de dynamiek van de atmosferische methaanconcentratie
Studie vindt de vingerafdruk van padie in de dynamiek van de atmosferische methaanconcentratie Stijgende verzekeringskosten kunnen Amerikanen ervan overtuigen dat de risico's van klimaatverandering reëel zijn
Stijgende verzekeringskosten kunnen Amerikanen ervan overtuigen dat de risico's van klimaatverandering reëel zijn
Hoofdlijnen
- Wat zijn de delen van een gewervelde dieren?
- Hoe dicht zijn we bij het succesvol bewerken van genen in menselijke embryo's?
- Wat is gelatine -achtige mengsel dat in het celmembraan stroomt?
- Na zeventien jaar wachten verschijnen de krekels iets eerder in de omgeving van Chicago:het is een mijlpaal
- Wat zijn voorbeelden van wetenschappelijke conclusies?
- Nieuwe mierenvogelsoort ontdekt in Peru
- Noem de zeven eigenschappen die alle levende organismen delen?
- Welk deel van plantencel dat sterkte en stijfheid biedt?
- Hoe lijken lysosomen vacuolen en plastiden op elkaar?
- Onderzoekers synthetiseren antimalariamoleculen gevonden in een schimmel uit Nunavut

- Onderzoeksteam ontdekt gebruik van elasticiteit om microplaten op gebogen 2D-vloeistoffen te positioneren
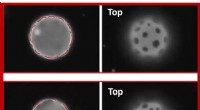
- Chemicus creëert katalysator om anti-muggenstoffen te produceren
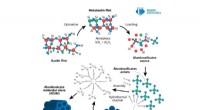
- Wetenschappers bieden bedrijven een nieuwe chemie voor groener polyurethaan

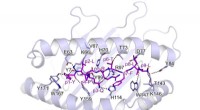
- Ontdekken hoe T-cellen het SARS-COV-2 virus spike-eiwit herkennen
 Soorten Schorpioenen Native to Colorado
Soorten Schorpioenen Native to Colorado  Hoeveel absilmijnen zijn volledig bezet in het tweede belangrijkste energieniveau van een grondstaat van natriumatoom?
Hoeveel absilmijnen zijn volledig bezet in het tweede belangrijkste energieniveau van een grondstaat van natriumatoom?  Hoe worden twee soorten cellen genoemd?
Hoe worden twee soorten cellen genoemd?  Frankrijk duwt Japan om fusie Renault-Nissan te accepteren:rapporten
Frankrijk duwt Japan om fusie Renault-Nissan te accepteren:rapporten Wat zijn contactkrachten en welk contact?
Wat zijn contactkrachten en welk contact?  Japan zet zich schrap voor zeer gevaarlijke tyfoon Nanmadol
Japan zet zich schrap voor zeer gevaarlijke tyfoon Nanmadol Hoe creëert een ster licht?
Hoe creëert een ster licht?  Waarom het zo moeilijk is om schepen bij te houden die niets goeds doen?
Waarom het zo moeilijk is om schepen bij te houden die niets goeds doen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

