
Wetenschap
Hoe oxideer je methaan?
1. Verbranding:
* proces: Dit is de meest eenvoudige manier om methaan te oxideren, waarbij het wordt verbrand in aanwezigheid van zuurstof.
* reactie:
CH4 + 2O2 → CO2 + 2H2O
* Uitkomst: Deze exotherme reactie produceert koolstofdioxide (CO2) en water (H2O) als primaire producten, samen met een aanzienlijke hoeveelheid warmte -energie.
* Toepassingen: Deze methode wordt veel gebruikt voor het genereren van elektriciteit in energiecentrales, evenals voor het verwarmen van huizen en industrieën.
2. Katalytische oxidatie:
* proces: Deze methode maakt gebruik van een katalysator om de oxidatie van methaan bij lagere temperaturen en druk te vergemakkelijken in vergelijking met verbranding.
* reactie: Afhankelijk van de katalysator en omstandigheden kunnen verschillende producten worden verkregen, waaronder:
* Gedeeltelijke oxidatie:
CH4 + 1.5O2 → CO + 2H2O
* Deze reactie produceert koolmonoxide (CO) en water, een belangrijke stap in de productie van synthesegas.
* Volledige oxidatie:
CH4 + 2O2 → CO2 + 2H2O
* Deze reactie levert koolstofdioxide en water op.
* Selectieve oxidatie:
CH4 + O2 → CH3OH + H2O
* Onder specifieke omstandigheden kan methanol (CH3OH) worden geproduceerd.
* katalysatoren: Verschillende metaaloxiden, zeolieten en ondersteunde metaalkatalysatoren worden gebruikt voor katalytische oxidatie van methaan.
* Toepassingen: Katalytische oxidatie wordt gebruikt in verschillende industriële processen, waaronder:
* Synthese -gasproductie: Voor de productie van brandstoffen, chemicaliën en meststoffen.
* methanolproductie: Gebruikt als brandstof en een uitgangsmateriaal voor veel chemische processen.
* Luchtvervuilingscontrole: Katalytische converters in voertuigen gebruiken dit proces om schadelijke verontreinigende stoffen te oxideren.
Andere oxidatiemethoden:
* Elektrochemische oxidatie: Deze methode omvat het gebruik van elektriciteit om methaan te oxideren in een elektrolytische cel.
* Fotokatalytische oxidatie: Gebruikt lichte energie en een fotokatalysator om methaan te oxideren.
factoren die oxidatie beïnvloeden:
* Temperatuur: Hogere temperaturen verhogen in het algemeen de oxidatiesnelheid.
* Zuurstofconcentratie: Een hogere zuurstofconcentratie verhoogt de reactiesnelheid.
* katalysatoractiviteit: Het type en de activiteit van de katalysator kan de reactiesnelheid en productselectiviteit aanzienlijk beïnvloeden.
* Druk: Hogere druk kan bepaalde oxidatiereacties bevorderen.
Inzicht in deze verschillende methoden en factoren zorgt voor gerichte oxidatie van methaan om specifieke producten te produceren op basis van gewenste toepassingen.
 Hoe weten wetenschappers over de structuur van het interieur?
Hoe weten wetenschappers over de structuur van het interieur?  NASA ontdekt dat het metrogebied van Virginia ongelijk aan het zinken is
NASA ontdekt dat het metrogebied van Virginia ongelijk aan het zinken is Kan het opwekken van mammoeten helpen om de uitstoot in het Noordpoolgebied te stoppen?
Kan het opwekken van mammoeten helpen om de uitstoot in het Noordpoolgebied te stoppen? Welke dieren leeft in de struikgewas van een regenwoud?
Welke dieren leeft in de struikgewas van een regenwoud?  Opwarming van de aarde verduistert nucleaire oorlog als grootste zorg:Nobelprijswinnaar
Opwarming van de aarde verduistert nucleaire oorlog als grootste zorg:Nobelprijswinnaar
Hoofdlijnen
- Veel soorten algen hebben welke organisatie?
- Waarom genoombewerking een gerichte manier biedt om betere gewassen te veredelen
- Designer biosensor kan de productie van antibiotica door microben detecteren
- Wie bestudeert de Whater -cyclus?
- Onderzoek naar maïsgenetica onthult het mechanisme achter het stil worden van eigenschappen
- Vier belangrijke typen chromosomen
- Ontdekking van een potentieel therapeutisch doelwit om trypanosomen te bestrijden
- Hoe en waarom is het oog voortgekomen door natuurlijke selectie?
- Hoe meten we pijn?
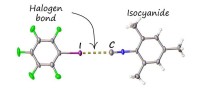
- Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden
- Onderzoekers ontwikkelen smartphonelezer voor snellere infectietests

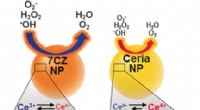
- Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis
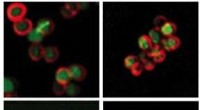
- Wetenschappers vinden krachtig potentieel wapen om antibioticaresistentie te overwinnen
- Zachte en ionengeleidende kunsttong van hydrogel voor astringentieperceptie

 Welk gebied duidt op een dramatische afname van materiaaldichtheid in de aarde?
Welk gebied duidt op een dramatische afname van materiaaldichtheid in de aarde?  Wat is Living Rock?
Wat is Living Rock?  Is zand een niet -metaal of metaal?
Is zand een niet -metaal of metaal?  Wat zijn enkele woorden van ademhalingssystemen die beginnen met de K?
Wat zijn enkele woorden van ademhalingssystemen die beginnen met de K?  Steden en landen streven ernaar om binnen tien jaar plastic afval te verminderen
Steden en landen streven ernaar om binnen tien jaar plastic afval te verminderen Ongeveer de helft van de hydraulisch gebroken putten bevindt zich binnen 2 tot 3 kilometer van huishoudelijke grondwatersystemen:studie
Ongeveer de helft van de hydraulisch gebroken putten bevindt zich binnen 2 tot 3 kilometer van huishoudelijke grondwatersystemen:studie Een object is noch versnellen of vertragen door reistjes naar een?
Een object is noch versnellen of vertragen door reistjes naar een?  Onderzoekers analyseren de uitdagingen waarmee contentmoderators tijdens een pandemie worden geconfronteerd
Onderzoekers analyseren de uitdagingen waarmee contentmoderators tijdens een pandemie worden geconfronteerd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

