
Wetenschap
Hoeveel covalente bindingen van 1 atoomstikstof met positieve netto lading kunnen vormen?
Inzicht in de basis
* Elektronenconfiguratie van stikstof: Stikstof heeft 5 valentie -elektronen (elektronen in de buitenste schaal).
* Covalente bindingen: Covalente bindingen vormen zich wanneer atomen elektronen delen om een stabiel octet (8 elektronen) in hun buitenste schaal te bereiken.
* Positieve lading: Een positieve netto lading op een atoom betekent dat het een of meer elektronen heeft verloren.
het toepassen van de concepten
1. Stikstof met een positieve lading: Als stikstof een positieve netto lading heeft, heeft dit een of meer elektronen verloren. Dit betekent dat er minder dan 5 valentie -elektronen beschikbaar zijn voor binding.
2. Bindingscapaciteit: Een stikstofatoom met een positieve lading zal een lagere bindingscapaciteit hebben. Een stikstofion met een +1 lading (N⁺) zou bijvoorbeeld slechts 4 valentie -elektronen beschikbaar hebben voor binding.
Conclusie
Een stikstofatoom met een positieve netto lading kan minder covalente bindingen vormen dan een neutraal stikstofatoom. Het exacte aantal bindingen hangt af van de grootte van de positieve lading.
Voorbeeld
* n⁺ (stikstof met +1 lading): Kan 3 covalente bindingen vormen.
* n²⁺ (stikstof met +2 lading): Kan 2 covalente bindingen vormen.
Belangrijke opmerking: De stabiliteit van deze bindingen zal afhangen van het specifieke molecuul en de andere betrokken atomen.
 Wateronderzoek ontdekt ontzilting van lokale stromen
Wateronderzoek ontdekt ontzilting van lokale stromen Wat zijn regenwolken?
Wat zijn regenwolken?  Wat is de betekenis van het begrijpen van hoe de aarde eruit ziet in relatie tot inspanningen voor milieubehoud?
Wat is de betekenis van het begrijpen van hoe de aarde eruit ziet in relatie tot inspanningen voor milieubehoud?  Hoe zit het met materie kan veranderen en wat is niet volgens de wet van natuurbehoud?
Hoe zit het met materie kan veranderen en wat is niet volgens de wet van natuurbehoud?  Waarom groeien bomen in het voorjaar?
Waarom groeien bomen in het voorjaar?
Hoofdlijnen
- Wat zijn twee manieren waarop pathogene organismen ziekte of infectie kunnen veroorzaken?
- Wat is het verschil tussen autotrofe en heterotrofe cellen?
- Klonten als tijdelijke opslag
- Wat zijn abiotische delen van een ecosysteem?
- Wat is een eencellige organismen?
- Welke vormreceptorsites op het post -synaptische celmembraan?
- Wat is de kleinste overervingseenheid?
- Wat is het verschil tussen een wetenschapper en onderzoeker?
- Waarom zijn pygmeeën klein?
- Wetenschappers vinden moleculaire vernietigingscode voor enzym dat betrokken is bij cholesterolproductie

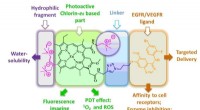
- Nieuwe zeer selectieve antitumor fotodynamische therapiemiddelen gesynthetiseerd
- Warmtegeleidend plastic kan leiden tot lichtere elektronica, auto's

- Het begrijpen van mortel van keramische materialen kan manieren onthullen om ze te verbeteren
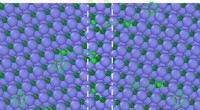
- Close-ups van korrelgrenzen onthullen hoe zwavelonzuiverheden nikkel broos maken

 NASA-missie om technologie voor satellietzwermen te testen
NASA-missie om technologie voor satellietzwermen te testen Onderzoekers vinden techniek voor 3D-printen op nanoschaal die fouten kan corrigeren
Onderzoekers vinden techniek voor 3D-printen op nanoschaal die fouten kan corrigeren In een prostar zal de kernfusie van waterstof beginnen wanneer?
In een prostar zal de kernfusie van waterstof beginnen wanneer?  Wat deden Hooke en Leewenhoek bij hun ontdekking van cellen?
Wat deden Hooke en Leewenhoek bij hun ontdekking van cellen?  Waarom zijn er extra onderdelen in een plantencel?
Waarom zijn er extra onderdelen in een plantencel?  Wat zijn enkele landvormen gemaakt door depositie?
Wat zijn enkele landvormen gemaakt door depositie?  Video:Hoe de houdbaarheidsdatum van medicijnen werkt
Video:Hoe de houdbaarheidsdatum van medicijnen werkt Wat is de vierde fase van een ster?
Wat is de vierde fase van een ster?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

