
Wetenschap
Wat is de naam van samengestelde FE2O2?
Dit is waarom:
* IJzer (Fe) heeft meerdere oxidatietoestanden: IJzer kan bestaan als fe²⁺ (ferro) of Fe³⁺ (ferrisch).
* zuurstof (O) heeft meestal een oxidatietoestand van -2: Zuurstof vormt bijna altijd een oxide -ion met een lading van -2.
Om ladingen in evenwicht te brengen, zijn de meest voorkomende ijzeroxiden:
* ijzer (ii) oxide (FeO): Dit heeft één fe²⁺ -ion en één o²⁻ ion.
* ijzer (iii) oxide (fe₂o₃): Dit heeft twee Fe³⁺ -ionen en drie o²⁻ -ionen.
Het is belangrijk om te onthouden dat chemische formules zijn gebaseerd op het in evenwicht brengen van ladingen tussen elementen. Fe₂o₂ zou een +4 lading vereisen op elk ijzeratoom, dat geen typische oxidatietoestand is voor ijzer.
 De reactie tussen zwaveltrioxide en water wordt genoemd?
De reactie tussen zwaveltrioxide en water wordt genoemd?  Hoe bereken je de ouder- en dochterisotopen om de fractie atomen te vinden die in een fossiel achterblijven?
Hoe bereken je de ouder- en dochterisotopen om de fractie atomen te vinden die in een fossiel achterblijven?  Machine learning voor zonne-energie is een supercomputer-killer
Machine learning voor zonne-energie is een supercomputer-killer Wat is een eigenschap van zowel de vaste toestand als de vloeibare toestand?
Wat is een eigenschap van zowel de vaste toestand als de vloeibare toestand?  Handige meting van de antioxidantcapaciteit van voedsel
Handige meting van de antioxidantcapaciteit van voedsel
 Welke wetenschappers bestuderen bugs?
Welke wetenschappers bestuderen bugs?  Ze kwamen met een nieuwe reeks doelen om de natuurlijke wereld te beschermen. Hier is hoe
Ze kwamen met een nieuwe reeks doelen om de natuurlijke wereld te beschermen. Hier is hoe Wat is een voorbeeld van een natuurlijke hulpbron op het land?
Wat is een voorbeeld van een natuurlijke hulpbron op het land?  Istanbul:zeebodemstudie bewijst voor het eerst het risico op aardbevingen
Istanbul:zeebodemstudie bewijst voor het eerst het risico op aardbevingen De pirarucu:de gigantische gewaardeerde vis van de Amazone
De pirarucu:de gigantische gewaardeerde vis van de Amazone
Hoofdlijnen
- Waar vinden de celreacties plaats?
- Hoe een dinosaurus te wegen
- Wat is het belangrijkste deel van DNA?
- Hoe wolvenpersoonlijkheden wetlands kunnen veranderen
- Hoe de hormonen van de hypofyse te onthouden
- Wat betekent ‘Kaukasisch’ werkelijk?
- Hoe weet een bacterie dat het tijd is om zich te splitsen?
- Nieuw hulpmiddel onthult hoe de verschillende vormen van organismen groeien
- Een schimmel die brood opstrijdt, wordt gebeld?
- Na een eeuw zoeken, wetenschappers vinden nieuwe vloeibare fase

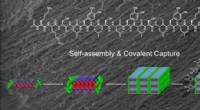
- Chemici ontwikkelen hydrogelsnaren met behulp van verbindingen die in zeedieren worden gevonden
- Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten

- Nieuwe route naar CO2-neutrale brandstoffen uit kooldioxide ontdekt

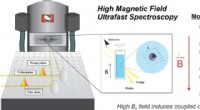
- Scholes vindt nieuw magnetisch veldeffect in diamagnetische moleculen
 Hawaï stopt met steenkool om klimaatverandering tegen te gaan
Hawaï stopt met steenkool om klimaatverandering tegen te gaan Wanneer babyplaneten smelten:op zoek naar de geschiedenis van planetesimalen
Wanneer babyplaneten smelten:op zoek naar de geschiedenis van planetesimalen Massive Angel Oak is getuige geweest van 500 jaar geschiedenis van South Carolina
Massive Angel Oak is getuige geweest van 500 jaar geschiedenis van South Carolina  Harpoen van koolstofnanobuisjes vangt individuele hersencelsignalen op
Harpoen van koolstofnanobuisjes vangt individuele hersencelsignalen op Stopt de moleculaire beweging als de diffusie stopt?
Stopt de moleculaire beweging als de diffusie stopt?  Waarom verschijnen groene planten voor ons?
Waarom verschijnen groene planten voor ons?  Wat voor soort energie is vereist om een lamp te laten werken?
Wat voor soort energie is vereist om een lamp te laten werken?  Wat is de belangrijkste processenergie die wordt overgedragen door de koperen muur van watertank?
Wat is de belangrijkste processenergie die wordt overgedragen door de koperen muur van watertank?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

