
Wetenschap
Wat is de molariteit van een oplossing die is bereid door 2,41 g kaliumjodide ki in 100 ml water op te lossen?
Hier leest u hoe u de molariteit van de kaliumjodide -oplossing kunt berekenen:
1. Bereken de mol ki:
* Molaire massa ki:
* K (kalium) =39,10 g/mol
* I (jodium) =126,90 g/mol
* Totale molaire massa =39,10 + 126,90 =166,00 g/mol
* mol ki:
* mol =massa / molaire massa
* mol =2,41 g / 166,00 g / mol =0,0145 mol
2. Converteer volume naar liters:
* Volume in liters: 100 ml =0,100 l
3. Molariteit berekenen:
* molariteit (m) =mol opgeloste stof / liters van oplossing
* molariteit =0,0145 mol / 0,100 l =0,145 m
Daarom is de molariteit van de kaliumjodide -oplossing 0,145 m.
 Verwanten van de Zebra
Verwanten van de Zebra Studie:Droogte brekende regens zeldzamer, grillig in het westen van de VS
Studie:Droogte brekende regens zeldzamer, grillig in het westen van de VS Beperking van klimaatverandering niet de belangrijkste drijfveer bij regeneratieve veeteelt
Beperking van klimaatverandering niet de belangrijkste drijfveer bij regeneratieve veeteelt Verduurzaming van fracken via innovaties in afvalwaterbeheer
Verduurzaming van fracken via innovaties in afvalwaterbeheer Californische boerderijregio geteisterd door vuile lucht kijkt naar Trump
Californische boerderijregio geteisterd door vuile lucht kijkt naar Trump
Hoofdlijnen
- Wat is de fase van mitose waar chromosomen lijnen in het midden?
- Wat voor soort vervuiling is een onderzoekslaboratoriumwetenschapper onzorgvuldig giet culturen die microben leven in de afvoer?
- Nieuwe inzichten in het gedrag van jonge doornenkroonsterren dat riffen bedreigt
- Waarom kunnen koolstofdioxide en water door het celmembraan gaan maar geen zetmeel -eiwitten?
- Ziek dolfijnkalf verbetert met sondemelk, helpende handen
- Eiwitten in haaientanden kunnen duiden op wat ze eten
- Welk twee orgaan reguleert het lichaamssysteem het meest direct?
- Waarom wordt virus niet opgenomen in het micro -organisme?
- Doel van pepsine in DNA -extract?
- Onderzoekers onthullen in-situ manipulatie van actieve goud-titaniumdioxide-interface

- Is er leven ontstaan in de oersoep via DNA of RNA? Misschien allebei

- Moleculaire dispersie verbetert quasi-dubbellaagse organische zonnecellen

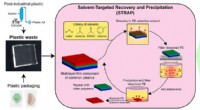
- Nieuw recyclingproces op basis van oplosmiddelen kan miljoenen tonnen plastic afval verminderen
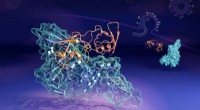
- Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad
 Duitsland geeft grafgeplunderde kunstvoorwerpen terug aan Alaska
Duitsland geeft grafgeplunderde kunstvoorwerpen terug aan Alaska Populieren die genetisch zijn gemodificeerd om de luchtkwaliteit niet te schaden, groeien net zo goed als niet-gemodificeerde bomen
Populieren die genetisch zijn gemodificeerd om de luchtkwaliteit niet te schaden, groeien net zo goed als niet-gemodificeerde bomen Het sleep-een-ijsbergplan wordt gelanceerd om de droogte in Kaapstad te verlichten
Het sleep-een-ijsbergplan wordt gelanceerd om de droogte in Kaapstad te verlichten Wat maakt stollingsrotsen verschillende kristalgroottes?
Wat maakt stollingsrotsen verschillende kristalgroottes?  Hoe worden staking-slip bergen gevormd?
Hoe worden staking-slip bergen gevormd?  PPPL bestudeert de rol van plasma's bij het synthetiseren van nanodeeltjes
PPPL bestudeert de rol van plasma's bij het synthetiseren van nanodeeltjes Kunnen gaswetten worden gebruikt met gebalanceerde chemische vergelijkingen om de hoeveelheid van een gasvormige reactant of product in reactie te berekenen?
Kunnen gaswetten worden gebruikt met gebalanceerde chemische vergelijkingen om de hoeveelheid van een gasvormige reactant of product in reactie te berekenen?  Wat is de ultieme bestemming van elektronen die van glucose zijn ontdaan?
Wat is de ultieme bestemming van elektronen die van glucose zijn ontdaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

