
Wetenschap
Wanneer een mol natriumchloride in water dissocieert, produceert het wat?
Wanneer een mol natriumchloride (NaCl) in water dissocieert, produceert deze:
* Eén mol natriumionen (Na+)
* Eén mol chloride-ionen (Cl-)
De dissociatiereactie ziet er zo uit:
NaCl (s) → Na + (aq) + Cl- (aq)
Hier is een uitsplitsing:
* NaCl (s): Vast natriumchloride
* Na+ (aq): Natriumionen opgelost in water (waterig)
* Cl- (aq): Chloride -ionen opgelost in water (waterig)
Dit is de reden waarom natriumchloride -oplossingen elektriciteit kunnen leiden, omdat de opgeloste ionen vrij kunnen bewegen en lading kunnen dragen.
 Het rioolwater van Tijuana beukte vorig jaar op de stranden van South Bay. EPA zegt dat er hulp onderweg is
Het rioolwater van Tijuana beukte vorig jaar op de stranden van South Bay. EPA zegt dat er hulp onderweg is Meta-analyse maakt duidelijk hoe functionele eigenschappen van fijne wortels reageren op experimentele opwarming van houtachtige planten
Meta-analyse maakt duidelijk hoe functionele eigenschappen van fijne wortels reageren op experimentele opwarming van houtachtige planten  Lijst van bedreigde dieren in de woestijn
Lijst van bedreigde dieren in de woestijn  Tyfoon Shanshan klemt Japanse kust vast, Tokio sparen
Tyfoon Shanshan klemt Japanse kust vast, Tokio sparen Steenkool is op weg om volledig onverzekerbaar te worden
Steenkool is op weg om volledig onverzekerbaar te worden
Hoofdlijnen
- Wat zijn de delen van een limaboon?
- Met behulp van neutronen bestuderen hoe resistente bacteriën evolueren
- Wat hebben somatische cellen en gameten met elkaar gemeen?
- Ambtenaren:GGO-muggen zijn geen drugs, EPA-toezicht nodig
- Hoe doen wetenschappers onderzoek?
- Waarom is het goed voor een organisme om meer oppervlakte te hebben?
- Wat is het woord voor prokaryoten met extremofielen orangnisme leven extreme omstandigheden?
- Waar zijn saprofyten gevestigd?
- Welke chemische stof die door mensen wordt gebruikt om bacteriën in drinkwater te doden, kan kanker zijn?
- Duurzame nylonproductie mogelijk gemaakt door ontdekking van bacteriën

- Ingenieurs bouwen chemisch aangedreven wielen die veranderen in tandwielen om mechanisch werk uit te voeren

- Machine learning stimuleert de zoektocht naar superharde materialen

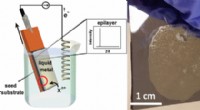
- Een goedkopere, groenere manier om kristallijne halfgeleiderfilms te kweken
- Hoe worden eiwitklitten zo lang bij Alzheimer?
 Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen
Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen Welk land heeft de meest historisch actieve vulkanen?
Welk land heeft de meest historisch actieve vulkanen?  Chimpansees:alarmoproepen met opzet?
Chimpansees:alarmoproepen met opzet?  Wat gebeurt er als er geen meting is?
Wat gebeurt er als er geen meting is?  Laat kommer en kwel vallen:klimaatjournalistiek gaat over empowerment
Laat kommer en kwel vallen:klimaatjournalistiek gaat over empowerment Kwantumsimulatietechniek levert topologische solitontoestand op in SSH-model
Kwantumsimulatietechniek levert topologische solitontoestand op in SSH-model Het dark web verlichten
Het dark web verlichten Gaat verwarming natriumchloride resulteren in een chemische verandering?
Gaat verwarming natriumchloride resulteren in een chemische verandering?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

