
Wetenschap
Hoeveel moleculen LiCl bevinden zich in een monster van 127,17 g?
1. Vind de molaire massa van LiCl:
* Li (lithium) heeft een molaire massa van 6,941 g/mol
* Cl (chloor) heeft een molaire massa van 35,453 g/mol
* Molaire massa van licl =6.941 g/mol + 35.453 g/mol =42.394 g/mol
2. Bereken het aantal mol Licl:
* Mol =massa / molaire massa
* Mol =127.17 g / 42.394 g / mol =3,00 mol
3. Gebruik het nummer van Avogadro om het aantal moleculen te vinden:
* Avogadro's nummer =6.022 x 10^23 moleculen/mol
* Aantal moleculen =mollen * Avogadro's nummer
* Aantal moleculen =3,00 mol * 6.022 x 10^23 moleculen/mol =1,81 x 10^24 moleculen
Daarom zijn er ongeveer 1,81 x 10^24 moleculen licl in een monster van 127,17 g.
 Wat is de evenwichtige vergelijking voor stikstofmonoxide plus koolstof is gelijk aan dioxide?
Wat is de evenwichtige vergelijking voor stikstofmonoxide plus koolstof is gelijk aan dioxide?  Stoomdistillatie versus eenvoudige destillatie
Stoomdistillatie versus eenvoudige destillatie  Welke formule en naam van de chemische stof verkocht als ijsmelt?
Welke formule en naam van de chemische stof verkocht als ijsmelt?  Beschrijf de algemene locatie van elektronen in een covalente binding?
Beschrijf de algemene locatie van elektronen in een covalente binding?  Verschil tussen homogeen en niet -materialen?
Verschil tussen homogeen en niet -materialen?
Hoofdlijnen
- FReD kan helpen verklaren hoe een bij ziet
- Wetenschappers identificeren hoe de ontwikkeling van verschillende soorten dezelfde genen met verschillende kenmerken gebruikt
- Nu Skype voor ons kan vertalen, waarom zou je een taal leren?
- Wat is het voordeel van het gebruik van wetenschappelijke namen in plaats daarvan gebruikelijk zoals kat of hond?
- Niet-vasculaire plant: definitie, kenmerken, voordelen en voorbeelden
- Honden en wolven delen parasieten
- Oceaanmonumenten worden geconfronteerd met mogelijk verlies van bescherming
- Verschillen en overeenkomsten tussen Unicellular & Cellular
- Welke elementen zijn bij mensen?
- Wetenschappers vinden schadelijke chemicaliën in huishoudstof

- Groene waterstof:onderzoek om efficiëntie te verhogen

- Een nieuwe manier om lichtgevoelige medicijnen te leveren om het probleem van antibioticaresistentie te bestrijden

- Parfummakers zoeken natuurlijke, duurzame geuren

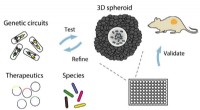
- Onderzoekers ontwikkelen nieuw platform dat kanker in een schaal nabootst om snel de beste bacteriële therapie te bepalen
 Welk pad lijkt de zon over de lucht te volgen?
Welk pad lijkt de zon over de lucht te volgen?  Wat zijn de belangrijkste geografische kenmerken van Israël?
Wat zijn de belangrijkste geografische kenmerken van Israël?  Hoe T-vormige clusters de scheiding van lanthaniden bevorderen tijdens vloeistof-vloeistofextractie
Hoe T-vormige clusters de scheiding van lanthaniden bevorderen tijdens vloeistof-vloeistofextractie  Wat is een niet-voorbeeld van korst?
Wat is een niet-voorbeeld van korst?  Onderzoekers ontwikkelen 3D-printbaar materiaal dat biologische weefsels nabootst
Onderzoekers ontwikkelen 3D-printbaar materiaal dat biologische weefsels nabootst Wat is de energiestroom als een ballon gevuld met lucht vrijgegeven?
Wat is de energiestroom als een ballon gevuld met lucht vrijgegeven?  Wat zijn de kosten van protonen, neutronen en elektronen?
Wat zijn de kosten van protonen, neutronen en elektronen?
Atomen zijn samengesteld uit drie verschillend geladen deeltjes: het positief geladen proton, het negatief geladen elektron en het neutrale neutron. De ladingen van het proton en elektron zi
 Hoogte berekenen uit volume
Hoogte berekenen uit volume
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

