
Wetenschap
Wat is de evenwichtige vergelijking voor stikstofmonoxide plus koolstof is gelijk aan dioxide?
De evenwichtige vergelijking voor stikstofmonoxide plus koolstof is gelijk aan koolstofdioxide en stikstof is:
2 NO + C → CO₂ + N₂
Dit is waarom:
* reactanten:
* Stikstofmonoxide (nee)
* Koolstof (C)
* Producten:
* Koolstofdioxide (co₂)
* Stikstof (n₂)
* balanceren:
* Er zijn 2 stikstofatomen aan de linkerkant en 2 aan de rechterkant.
* Er is 1 zuurstofatoom aan de linkerkant en 2 aan de rechterkant. Om dit in evenwicht te brengen, plaatsen we een coëfficiënt van 2 voor nr.
* Er is 1 koolstofatoom aan elke kant.
Deze vergelijking laat nu zien dat het aantal van elk type atoom hetzelfde is aan beide zijden van de reactie, waardoor het in evenwicht is.
 Hoe is het periodiek systeem georganiseerd?
Hoe is het periodiek systeem georganiseerd?  Waarom zijn een organische verbinding van aard gekleurd?
Waarom zijn een organische verbinding van aard gekleurd?  Waarom brandend metaal betekent reactie met zuurstof?
Waarom brandend metaal betekent reactie met zuurstof?  Nieuw bewijs toont aan dat de eerste bouwstenen van het leven op aarde misschien rommeliger waren dan eerder werd gedacht
Nieuw bewijs toont aan dat de eerste bouwstenen van het leven op aarde misschien rommeliger waren dan eerder werd gedacht Een eenvoudige manier om complexe halfgeleiders zichzelf te laten assembleren
Een eenvoudige manier om complexe halfgeleiders zichzelf te laten assembleren
 Hoe vakantiefoto's van zebra's en walvissen kunnen bijdragen aan natuurbehoud
Hoe vakantiefoto's van zebra's en walvissen kunnen bijdragen aan natuurbehoud  Waarom het Amerikaanse wapengeweld toeneemt bij warm weer
Waarom het Amerikaanse wapengeweld toeneemt bij warm weer  Beschrijf de theorie van natuurlijke selectie als de evolutie van het mechanisme?
Beschrijf de theorie van natuurlijke selectie als de evolutie van het mechanisme?  Wat zijn de drie belangrijkste manieren waarop ecosystemen kunnen worden gewijzigd?
Wat zijn de drie belangrijkste manieren waarop ecosystemen kunnen worden gewijzigd?  Hoe kom je van Stucco-etende vogels
Hoe kom je van Stucco-etende vogels
Hoofdlijnen
- Wat is een groep cellen die speciale chemicaliën voor je lichaam maken?
- Beschrijf hoe de cel van stengels gassen wisselen over hun barrières?
- Hoe stelt de structuur van microtubuli hen in staat om blijkbaar van de ene locatie een cel te verplaatsen?
- Hoe hebben Watson en Crick baseparing bepaald?
- Hersenorganoïden geven inzicht in de evolutie van het menselijk brein
- Wie heeft het eerste DNA -model gemaakt?
- Kan graszaad net zo goed groeien op een lavasteen als op aarde?
- Wat is watermassa?
- Nieuwe inzichten in hoe genen verkering en agressie beheersen
- Nieuwe zouten leggen de lat hoger voor lithium-ionbatterijtechnologie

- Polymeercoating versnelt de brandstofproductie

- Ultrakleine holle nanodeeltjes van legering voor synergetische katalyse van waterstofevolutie

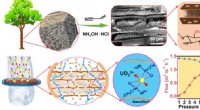
- Team ontdekt dat biologische nanofibrillen op efficiënte wijze waardevolle metaalelementen uit water kunnen halen
- Nieuwe katalysator met dubbele functie voor waterstof- en plasticproductie

 Hoe heet de grond die door rivieren wordt afgezet?
Hoe heet de grond die door rivieren wordt afgezet?  Cats Eye-nevel gezien in 3D
Cats Eye-nevel gezien in 3D Wat zijn enkele natuurkrachten?
Wat zijn enkele natuurkrachten?  Nieuwe tool om de bouwsector te helpen de ecologische voetafdruk te verkleinen
Nieuwe tool om de bouwsector te helpen de ecologische voetafdruk te verkleinen Aan de Caribische kust van Mexico groeien bergen zeewier
Aan de Caribische kust van Mexico groeien bergen zeewier Wat is een breuk en fout in de rotslaag?
Wat is een breuk en fout in de rotslaag?  Hoe kunnen zonnevlammen mogelijk elektronica vernietigen?
Hoe kunnen zonnevlammen mogelijk elektronica vernietigen?  Hoe kun je aan de zuurstofbehoefte komen?
Hoe kun je aan de zuurstofbehoefte komen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

