
Wetenschap
Wat is de evenwichtige vergelijking voor enkele vervangingsreactie van calciummetaal met waterige HCl om chloride en waterstofgas te vormen?
1. Identificeer de reactanten en producten:
* reactanten: Calciummetaal (CA) en zoutzuur (HCL)
* Producten: Calciumchloride (CaCl₂) en waterstofgas (H₂)
2. Schrijf de onevenwichtige vergelijking:
Ca (s) + HCl (aq) → CaCl₂ (aq) + h₂ (g)
3. Breng de vergelijking in evenwicht:
* calcium (CA): Eén CA -atoom aan elke kant, dus het is in balans.
* chloor (CL): Twee CL -atomen aan de productzijde (CaCl₂) en één aan de reactantzijde (HCL). Om in evenwicht te zijn, zet je een coëfficiënt van 2 voor HCl.
* waterstof (h): Twee H -atomen aan de productzijde (H₂) en twee aan de reactantzijde (2HCl), dus het is evenwichtig.
4. De evenwichtige vergelijking is:
Ca (s) + 2HCl (aq) → CaCl₂ (aq) + h₂ (g)
 Als voor 1,25 gram zuiver CaCO3 25,5 ml HCl-oplossing nodig is voor een volledige reactie, wat is dan de molariteitsoplossing?
Als voor 1,25 gram zuiver CaCO3 25,5 ml HCl-oplossing nodig is voor een volledige reactie, wat is dan de molariteitsoplossing?  Kun je eenvoudig vergelijken en contrasteren tegen stoomdestillatie in termen van type mengsels gescheiden?
Kun je eenvoudig vergelijken en contrasteren tegen stoomdestillatie in termen van type mengsels gescheiden?  Een verademing in de plasmonische katalyse:de renaissance van zwart goud en zonne-energie
Een verademing in de plasmonische katalyse:de renaissance van zwart goud en zonne-energie  Wetenschappers werken aan het maken van microchip-elementen van moleculaire grootte
Wetenschappers werken aan het maken van microchip-elementen van moleculaire grootte Waarom is 4 methylpyridine eenvoudiger?
Waarom is 4 methylpyridine eenvoudiger?
 John Deutch over realistische prognoses van economische groei en koolstofemissies
John Deutch over realistische prognoses van economische groei en koolstofemissies Enorme bosbranden treffen Zuid-Brazilië Pantanal
Enorme bosbranden treffen Zuid-Brazilië Pantanal Hoe kunt u landplanten op twee manieren classificeren?
Hoe kunt u landplanten op twee manieren classificeren?  Afwatering van veengebieden in Zuidoost-Azië draagt bij aan klimaatverandering
Afwatering van veengebieden in Zuidoost-Azië draagt bij aan klimaatverandering Een indianendorp vecht om de poep naar de wc te brengen
Een indianendorp vecht om de poep naar de wc te brengen
Hoofdlijnen
- Wat zijn de belangrijkste functies van het reproductieve systeem?
- Is het waar dat willekeurige paring tot micro-evolutie leidt?
- Welke oplossing veroorzaakt niet de netto beweging van water in of uit een rode bloedcel?
- Darmmicrobioom helpt beren met zeer verschillende diëten om dezelfde grootte te bereiken
- Hoe je toch een resistente parasiet kunt doden
- Wat zijn banden bij elektroforese?
- Wat is het verschil tussen producenten die fotosynthese en chemosynthese gebruiken?
- Nieuwe studie ontdekt klein doelwit op RNA om ontstekingen te kortsluiten
- Nieuwe ontdekking daagt lang gekoesterde evolutietheorie uit
- Nieuw antibioticum vernoemd naar Leiden

- Chemici synthetiseren psychotrope verbindingen uit regenwoudboom
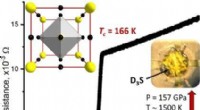
- Op weg naar conducteurs van de toekomst
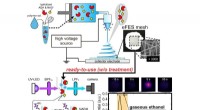
- Onderzoekers ontwikkelen een nieuwe manier om een spectrum van natuurlijk ogende haarkleuren te creëren

- Bouw van betere biosensoren in de gasfase voor de bestrijding van ziekten
 Streamen naar abonnementen:videogames betreden nieuwe grenzen
Streamen naar abonnementen:videogames betreden nieuwe grenzen Wat is de netto kracht op een dragster met een massa van 900 kg als zijn versnelling 32.0 MS2 West?
Wat is de netto kracht op een dragster met een massa van 900 kg als zijn versnelling 32.0 MS2 West?  Wereldwijde handel en consumptie van grondstoffen plaatsen de primaten ter wereld met uitsterven bedreigd
Wereldwijde handel en consumptie van grondstoffen plaatsen de primaten ter wereld met uitsterven bedreigd Wat zijn onderwaterorganismen?
Wat zijn onderwaterorganismen?  Wanneer geloof in de erfenis van gedragspatronen in combinatie is met het gevoel dat bepaalde groepen inherent superieur zijn aan anderen die het noemt?
Wanneer geloof in de erfenis van gedragspatronen in combinatie is met het gevoel dat bepaalde groepen inherent superieur zijn aan anderen die het noemt?  Aspirant-stedenbouwkundigen proberen gentrificatie in Pacoima . te verminderen
Aspirant-stedenbouwkundigen proberen gentrificatie in Pacoima . te verminderen Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers
Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers Wat zijn de namen van twee coördinaten op Celestial Sphere die worden gebruikt om te bepalen waar een ster zich bevindt?
Wat zijn de namen van twee coördinaten op Celestial Sphere die worden gebruikt om te bepalen waar een ster zich bevindt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

