
Wetenschap
Wat is de oxidatie of lading van ammonium?
Ammonium (NH₄⁺) heeft een +1 lading .
Dit is waarom:
* Elektronegativiteit van stikstof: Stikstof is elektronegatiefer dan waterstof, wat betekent dat het elektronen sterker aantrekt.
* Covalente bindingen: De bindingen tussen stikstof en waterstof in ammonium zijn covalent, wat betekent dat ze elektronen delen. De gedeelde elektronen worden echter dichter bij het stikstofatoom getrokken vanwege de hogere elektronegativiteit.
* Formele lading: Deze ongelijke delen van elektronen resulteert in een formele lading van +1 op het stikstofatoom.
* Algemeen lading: Omdat de vier waterstofatomen elk een neutrale lading hebben, is de algehele lading van ammonium +1.
 De limiet voor de opwarming van de aarde van 1,5 graad is niet onmogelijk, maar zal dat binnenkort wel worden
De limiet voor de opwarming van de aarde van 1,5 graad is niet onmogelijk, maar zal dat binnenkort wel worden Lava gutst uit vulkaan bij Manilla; tienduizenden vluchten
Lava gutst uit vulkaan bij Manilla; tienduizenden vluchten Goedkope sensoren meten realtime blootstelling aan vulkanische smog
Goedkope sensoren meten realtime blootstelling aan vulkanische smog Hoe beleid tegen wildgroei de waterkwaliteit kan schaden
Hoe beleid tegen wildgroei de waterkwaliteit kan schaden Het morele element van klimaatverandering
Het morele element van klimaatverandering
Hoofdlijnen
- Welke andere wetenschapper stelde een verkeerd idee voor maar de wetenschap bevorderde?
- Wat is de functie van het reproductieve systeem van de organen?
- Een samensmelting van microben:onderzoek toont aan dat omstandigheden met weinig voedingsstoffen de virale infectie veranderen
- Wat is micro-evolutie?
- Welk systeem verwijst witte materie naar gemyelineerde vezels?
- Wat is een enkel cel organisme dat alle levensprocessen kan voortzetten?
- Wat is een allel dat een eigenschap produceert in de heterozygote toestand is?
- De vraag naar zeevruchten stijgt enorm, maar de oceanen geven alles op wat ze kunnen. Kunnen we vis op nieuwe manieren kweken?
- Wat zijn de gespecialiseerde cellen die vasculair weefsel vormen?
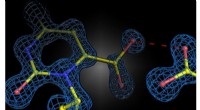
- Hoe gelijke ladingen in enzymen biochemische reacties regelen
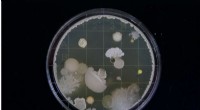
- Magnetische bacteriën als micropompen
- Wetenschappers gebruiken nanotechnologie om de prestaties van belangrijke industriële katalysatoren te verbeteren

- Neutronen onthullen de wilde Weyl-wereld van halfmetalen

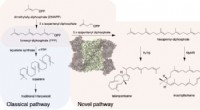
- Nieuw type triterpenen ontdekt
 Filippijnen kampt met leercrisis na jarenlange schoolsluiting
Filippijnen kampt met leercrisis na jarenlange schoolsluiting Hoeveel energie zit er in één batterij?
Hoeveel energie zit er in één batterij?  Hubble viert zijn 29e verjaardag met ongeëvenaard zicht op de Zuidelijke Krabnevel
Hubble viert zijn 29e verjaardag met ongeëvenaard zicht op de Zuidelijke Krabnevel Hoe maak je grafieken in Sigma-plot?
Hoe maak je grafieken in Sigma-plot?  Wat is een samengesteld gemiddelde in de wetenschap?
Wat is een samengesteld gemiddelde in de wetenschap?  Wetenschappers leggen live vast, detail op atomair niveau van de vorming van nanodeeltjes
Wetenschappers leggen live vast, detail op atomair niveau van de vorming van nanodeeltjes Amazon stuurt verder richting auto's, neemt GM executive aan
Amazon stuurt verder richting auto's, neemt GM executive aan Nieuwe niet-destructieve optische techniek onthult de structuur van parelmoer
Nieuwe niet-destructieve optische techniek onthult de structuur van parelmoer
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

