
Wetenschap
Waarom kan een onevenwichtige chemische vergelijking een reactie niet volledig beschrijven?
1. Schending van de wet van het behoud van massa:
* Het fundamentele principe van chemie stelt dat materie niet kan worden gecreëerd of vernietigd in een chemische reactie.
* Een onevenwichtige vergelijking suggereert dat atomen verdwijnen of uit dunne lucht verschijnen, wat onmogelijk is.
2. Onjuiste stoichiometrie:
* Stoichiometrie is de studie van de kwantitatieve relaties tussen reactanten en producten in chemische reacties.
* Een onevenwichtige vergelijking biedt geen informatie over de relatieve hoeveelheden reactanten en producten die bij de reactie betrokken zijn. Dit maakt het onmogelijk om de opbrengst van een reactie te voorspellen of om de hoeveelheid reactanten te berekenen die nodig is voor een specifieke hoeveelheid product.
3. Onnauwkeurige weergave van de reactie:
* Een evenwichtige vergelijking weerspiegelt nauwkeurig het aantal atomen van elk element aan beide zijden van de vergelijking.
* Een onevenwichtige vergelijking vertegenwoordigt niet nauwkeurig de werkelijke chemische veranderingen die tijdens de reactie plaatsvinden. Het kan leiden tot een misverstand van het reactiemechanisme en de gevormde producten.
4. Misleidende interpretatie van de reactie:
* Een onevenwichtige vergelijking kan een reactie suggereren die niet in werkelijkheid opkomt of de producten van een reactie ten onrechte voorspelt.
* Een onevenwichtige vergelijking kan bijvoorbeeld suggereren dat een enkele reactant meerdere producten produceert terwijl in werkelijkheid mogelijk meerdere reactanten vereisen of een andere set producten produceren.
Samenvattend is een evenwichtige chemische vergelijking cruciaal voor:
* Nauwkeurige weergave: Het weerspiegelt de werkelijke chemische veranderingen die plaatsvinden.
* Behoud van massa: Het houdt zich aan het fundamentele principe van behoud van massa.
* voorspellende kracht: Hiermee kunnen we de hoeveelheid reactanten en producten voorspellen.
* Inzicht in de reactie: Het biedt een duidelijk beeld van de chemische transformaties.
Daarom is een onevenwichtige vergelijking een onvolledige en mogelijk misleidende weergave van een chemische reactie. Het is essentieel om chemische vergelijkingen in evenwicht te brengen om de reacties volledig te begrijpen en te beschrijven.
 Hoeveel mol KNO3 moet in totaal in water worden opgelost om van 1,5 liter een stroom van 2,0 M te maken?
Hoeveel mol KNO3 moet in totaal in water worden opgelost om van 1,5 liter een stroom van 2,0 M te maken?  Ontwikkeld enzym dat PET in tien uur kan afbreken
Ontwikkeld enzym dat PET in tien uur kan afbreken Hydrogel coating is de eerste om ijsvorming op 3 verschillende manieren te voorkomen
Hydrogel coating is de eerste om ijsvorming op 3 verschillende manieren te voorkomen Wat zou er gebeuren met de concentratie van waterstofionen in een oplossing sterk zuur als een gelijk aantal hydroxide werd toegevoegd?
Wat zou er gebeuren met de concentratie van waterstofionen in een oplossing sterk zuur als een gelijk aantal hydroxide werd toegevoegd?  Wetenschappers ontwikkelen nieuwe transparante breedband afschermende materialen voor elektromagnetische interferentie
Wetenschappers ontwikkelen nieuwe transparante breedband afschermende materialen voor elektromagnetische interferentie
 De dreiging die uitgaat van klimaatverandering:uit onderzoek blijkt dat ouders ouder dan 40 jaar zich net zoveel zorgen maken als niet-ouders
De dreiging die uitgaat van klimaatverandering:uit onderzoek blijkt dat ouders ouder dan 40 jaar zich net zoveel zorgen maken als niet-ouders  Algoritme biedt systeem voor vroegtijdige waarschuwing voor het volgen van grondwaterverontreiniging
Algoritme biedt systeem voor vroegtijdige waarschuwing voor het volgen van grondwaterverontreiniging Veranderingen in de regenseizoenen in Zuid-Afrika kunnen gevolgen hebben voor de landbouw en de watervoorraden
Veranderingen in de regenseizoenen in Zuid-Afrika kunnen gevolgen hebben voor de landbouw en de watervoorraden Opwarming van de aarde tegengaan door CO2-opslag? Controleer op continentale stress
Opwarming van de aarde tegengaan door CO2-opslag? Controleer op continentale stress Waarschuwingssysteem heeft mogelijk levens gered in Indonesische tsunami
Waarschuwingssysteem heeft mogelijk levens gered in Indonesische tsunami
Hoofdlijnen
- De vijand binnenin:hoe ziekteverwekkers zich ongemerkt in het lichaam verspreiden
- Hoe big data uit sociale media ons helpt de dynamiek beter te begrijpen
- Carrier -eiwitten vereisen geen energie om aminozuren in een cel te transporteren?
- Kan een kleine invasieve slak Latijns-Amerikaanse koffie helpen redden?
- Hoe mensen en hun darmmicroben kunnen reageren op plantenhormonen
- Twee studies vinden dat stress cellen herprogrammeert
- Onderzoek toont gedragsveranderingen, fysiologische veranderingen bij mieren die verstoord zijn door ontwikkeling, stadsuitbreiding
- Belangrijke foerageerplaatsen voor onechte karetschildpadden geïdentificeerd
- Hoe reproduceert een lionfish zich?
- Nieuwe moleculen voor OLED's en geneesmiddelen

- De suikercode ontcijferen

- Organische kation-intercalatie:een effectieve strategie voor het manipuleren van bandtopologie en supergeleiding

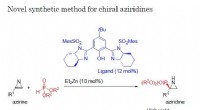
- Nieuwe chemische synthesemethode kan een opwindende reeks nieuwe verbindingen produceren
- Paddestoelen, veren combineren in biologisch afbreekbare schoenen

 Waarom hebben bergen lagere temperaturen dan vlaktes?
Waarom hebben bergen lagere temperaturen dan vlaktes?  Hoe maak je een 3D-model van het ademhalingssysteem
Hoe maak je een 3D-model van het ademhalingssysteem  Samsung lanceert opvouwbare smartphone na grote vertraging
Samsung lanceert opvouwbare smartphone na grote vertraging Stamcellen lijken sneller in de ruimte
Stamcellen lijken sneller in de ruimte Welke twee hoofdkenmerken beschrijven het weer?
Welke twee hoofdkenmerken beschrijven het weer?  Ondanks spanningen, De wijnindustrie van Turkije weigert te verwelken
Ondanks spanningen, De wijnindustrie van Turkije weigert te verwelken Hoe is frequentie gerelateerd aan snelheid?
Hoe is frequentie gerelateerd aan snelheid?  Wat is een chemische reactie en hoe gaat het om reactantenproducten?
Wat is een chemische reactie en hoe gaat het om reactantenproducten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

