
Wetenschap
Wat zou er gebeuren met de concentratie van waterstofionen in een oplossing sterk zuur als een gelijk aantal hydroxide werd toegevoegd?
De concentratie waterstofion zou afnemen.
Verklaring:
* Sterke zuren: Sterke zuren ioniseren volledig in oplossing, wat betekent dat ze al hun waterstofionen (H+) in de oplossing afgeven.
* Hydroxide -ionen: Hydroxide-ionen (OH-) zijn de basiscomponent van water. Het zijn sterke bases.
* neutralisatie: Wanneer een sterk zuur en een sterke basis reageren, neutraliseren ze elkaar. Dit betekent dat de waterstofionen (H+) van het zuur reageren met de hydroxide-ionen (OH-) van de basis om water (H2O) te vormen.
reactie:
H + (van zuur) + OH- (van basis) → H2O
Resultaat:
* De toevoeging van hydroxide -ionen zal direct waterstofionen in de oplossing consumeren, waardoor hun concentratie wordt verminderd.
* Aangezien het zuur en de basis reageren in een verhouding van 1:1, als u een gelijk aantal hydroxide -ionen toevoegt aan waterstofionen, wordt de oplossing neutraal.
* Als u meer hydroxide -ionen toevoegt dan waterstofionen, wordt de oplossing eenvoudig.
Belangrijke opmerking: De uiteindelijke pH van de oplossing hangt af van de initiële concentratie van het sterke zuur en de hoeveelheid toegevoegde hydroxide -ionen.
Hoofdlijnen
- Waar wordt Myelin gevonden en wat zijn functie?
- Wat maakt rode en witte bloedcellen?
- Wat is het gebruik van fotosynthsis en ademhaling?
- Wat is het chromosoom aantal suikerriet?
- Een protist die zijn eigen voedsel maakt, is een?
- Zijn eiwitten in een cel levend?
- Waarom onderzoekers denken dat sommige uitgestorven gigantische vliegende reptielen voor hun jongen zorgden
- Waar vindt aerobe ademhaling plaats in de cel?
- Hoe een zieke cel te resetten
- Nanofiltratiemembranen voor de behandeling van industrieel afvalwater van zware metalen

- Schorpioenen maken een fluorescerende stof die hen kan helpen beschermen tegen parasieten

- Biomedische ingenieurs maken slimme verbanden om chronische wonden te genezen

- Alternatieve cementrecepten - Een recept voor eco-beton

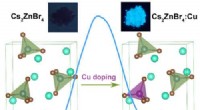
- Methode om blauw-emitterende nuldimensionale volledig anorganische metaalhalogeniden te ontwikkelen
 College.xxx? Scholen kopen pornodomeinen om ze schoon te houden
College.xxx? Scholen kopen pornodomeinen om ze schoon te houden  Wat maakt een goede werkhond? Een 'bekwaamheidstest' voor honden kan aanwijzingen bieden
Wat maakt een goede werkhond? Een 'bekwaamheidstest' voor honden kan aanwijzingen bieden  Hoeveel stenen is 64 kilogram?
Hoeveel stenen is 64 kilogram?  Casestudies laten zien hoe quasi-gouvernementele organisaties het beheer van klimaatadaptatie kunnen versterken
Casestudies laten zien hoe quasi-gouvernementele organisaties het beheer van klimaatadaptatie kunnen versterken  Hoe worden mineralen gevormd?
Hoe worden mineralen gevormd?  De natuur stelt nog steeds de norm voor de nanowetenschapsrevolutie
De natuur stelt nog steeds de norm voor de nanowetenschapsrevolutie Stephen Hawking geloofde niet dat hij naar de hemel zou gaan, een plek voor mensen die bang zijn in het donker
Stephen Hawking geloofde niet dat hij naar de hemel zou gaan, een plek voor mensen die bang zijn in het donker Warmer watersignalen veranderen voor Schotse shags
Warmer watersignalen veranderen voor Schotse shags
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


