
Wetenschap
Volledige ionische vergelijking voor CACL2 2AGNO3 - CANO32 2AGCL?
1. Evenwichtige chemische vergelijking:
CACL₂ (aq) + 2Agno₃ (aq) → Ca (no₃) ₂ (aq) + 2agcl (s)
2. Het identificeren van de ionen in oplossing:
* cacl₂ (aq): Ca²⁺ (aq) + 2cl⁻ (aq)
* Agno₃ (aq): Ag⁺ (aq) + no₃⁻ (aq)
* ca (no₃) ₂ (aq): Ca²⁺ (aq) + 2no₃⁻ (aq)
* agcl (s): Dit is een vast neerslag en dissocieert niet in ionen.
3. Volledige ionische vergelijking:
ca²⁺ (aq) + 2cl⁻ (aq) + 2ag⁺ (aq) + 2no₃⁻ (aq) → ca²⁺ (aq) + 2no₃⁻ (aq) + 2agcl (s)
Sleutelpunten:
* toeschouwersionen: Merk op dat ca²⁺ en no₃⁻ ionen aan beide zijden van de vergelijking verschijnen. Dit worden toeschouwersionen genoemd omdat ze niet direct deelnemen aan de reactie.
* Netto ionische vergelijking: Om ons te concentreren op de essentiële reactie, kunnen we de toeschouwersionen elimineren om de netto ionische vergelijking te krijgen:
2ag⁺ (aq) + 2cl⁻ (aq) → 2agcl (s)
Deze vergelijking vertegenwoordigt de vorming van het zilveren chloride -neerslag.
 Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen Hoe ontleden chemicaliën?
Hoe ontleden chemicaliën?  Wetenschappers ontdekken het mechanisme voor ethylcarbamaat-geïnduceerde toxiciteit in gefermenteerd voedsel
Wetenschappers ontdekken het mechanisme voor ethylcarbamaat-geïnduceerde toxiciteit in gefermenteerd voedsel Wat is het enige natuurlijk voorkomende element dat wordt gebruikt voor nucleaire splijting?
Wat is het enige natuurlijk voorkomende element dat wordt gebruikt voor nucleaire splijting?  Zijn waterstofbindingen sterk of zwak?
Zijn waterstofbindingen sterk of zwak?
Hoofdlijnen
- Wat zijn feiten die de evolutie weerleggen?
- Waar bevindt zich het diafragma op de microscoop?
- Hoe reproduceert een Yersinia -pestis zich?
- Betekent het neutraal liefhebben van een fagocyt?
- Hoe wordt het genoemd als wetenschapper de methode volgt?
- Wat voor soort bacteriën veroorzaakt ziekte?
- Waarom kunnen we ons niet herinneren dat we baby's waren?
- Welke organen zijn aan uw recht?
- Onderzoekers brachten twee jaar door in diepe ondergrondse grotten om dit buitengewone fossiel aan het licht te brengen
- Wetenschappers ontwerpen nieuwe eiwitstructuur
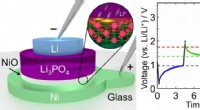
- Klein, snel, en zeer energiezuinig geheugenapparaat geïnspireerd op lithium-ionbatterijen
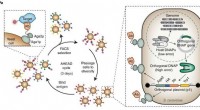
- Nieuwe tool is bedoeld om COVID-19 te bestrijden, andere ziekten
- Power-to-gas-installatie met hoog rendement

- De impact van de toename van afwijzingen van nieuwe medicijnen

 Maaien of niet maaien:Overlastgroei van waterplanten bij de wortel aanpakken
Maaien of niet maaien:Overlastgroei van waterplanten bij de wortel aanpakken Wanneer ze vanuit het noorden worden bekeken, draaien alle planeten rond de zon, de meeste van hen roteren in deze zin en hebben ze ook de meeste hun satellieten?
Wanneer ze vanuit het noorden worden bekeken, draaien alle planeten rond de zon, de meeste van hen roteren in deze zin en hebben ze ook de meeste hun satellieten?  Wat zijn de grondsoorten in zoetwaterbiomen?
Wat zijn de grondsoorten in zoetwaterbiomen?  Welk effect heeft de massa van het object op zijn momentum?
Welk effect heeft de massa van het object op zijn momentum?  Welke landvorm heeft zeer steile kanten?
Welke landvorm heeft zeer steile kanten?  methaanthiol, een potentiële nieuwe grondstof in de C1-chemie
methaanthiol, een potentiële nieuwe grondstof in de C1-chemie Zelfherstellende batterijen:ingenieurs ontwikkelen een manier om batterijen met een hoge capaciteit en een lange levensduur te maken
Zelfherstellende batterijen:ingenieurs ontwikkelen een manier om batterijen met een hoge capaciteit en een lange levensduur te maken Bestuderen van top-quarks met hoge en minder hoge energieën
Bestuderen van top-quarks met hoge en minder hoge energieën
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

