
Wetenschap
Hoeveel gram zuurstofgas is vereist om volledig te reageren met 14,6 vaste natriumvormige oxide?
1. Schrijf de gebalanceerde chemische vergelijking:
De reactie tussen natrium (NA) en zuurstof (O₂) om natriumoxide te vormen (Na₂o) is:
4 Na + o₂ → 2 na₂o
2. Bepaal de molaire massa van elke stof:
* NA:22,99 g/mol
* O₂:32,00 g/mol (zuurstof is diatomeeën)
* Na₂o:61,98 g/mol
3. Converteer gram natriumoxide in mol:
* Mol na₂o =(14,6 g na₂o) / (61,98 g / mol na₂o) =0,235 mol na₂o
4. Gebruik de molverhouding van de gebalanceerde vergelijking:
De gebalanceerde vergelijking laat zien dat 2 mol Na₂o wordt geproduceerd uit 1 mol o₂. We kunnen deze verhouding gebruiken om de mol O₂ nodig te vinden:
* Mol o₂ =(0,235 mol na₂o) * (1 mol o₂ / 2 mol na₂o) =0,118 mol o₂
5. Converteer mol zuurstof in gram:
* Gram van o₂ =(0.118 mol o₂) * (32,00 g/mol o₂) =3,78 g o₂
Daarom is 3,78 gram zuurstofgas vereist om volledig te reageren met 14,6 gram vast natrium om oxide te vormen.
 De VS waarschuwen voor een milieuramp als het vrachtschip wordt getroffen door Huthi-rebellen
De VS waarschuwen voor een milieuramp als het vrachtschip wordt getroffen door Huthi-rebellen  Welke dieren eten insecten in een regenwoud?
Welke dieren eten insecten in een regenwoud?  Bestaat er niet zoiets als een plasticvrije lunch?
Bestaat er niet zoiets als een plasticvrije lunch? Bossen kappen:geen eenvoudige oplossing voor bosbranden in Californië
Bossen kappen:geen eenvoudige oplossing voor bosbranden in Californië Waarom voelen liminale ruimtes zo verontrustend en toch vertrouwd aan?
Waarom voelen liminale ruimtes zo verontrustend en toch vertrouwd aan?
Hoofdlijnen
- Wat is de werkingslijn in de wetenschap?
- Wat betekent de term haploïde?
- Waarom zou een wetenschapper zijn hypothese heroverwegen?
- Wat is een verzameling organen die een specifieke functie voor het lichaam uitvoeren?
- Sluit Nike zich aan bij de selectie van Amazon?
- Wie kreeg de eerste Nobelprijs voor biologie?
- Waarom worden sommige aminozuren essentiële aminozuren genoemd?
- Het bestuderen van de ongelijkheid in rijkdom bij dieren kan aanwijzingen onthullen over hoe hun samenlevingen zich ontwikkelden
- Wat is het laagste niveau van biologische organisatie om kenmerken te hebben leven?
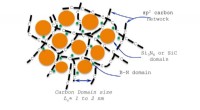
- Ingenieur patenteert waterachtig polymeer om keramiek op hoge temperatuur te maken
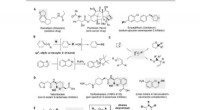
- Invoeging van boor in alkyletherbindingen via tandemkatalyse van zink/nikkel
- Wetenschappers ontwikkelen methode om fluorescerende biosensoren te testen voordat ze worden gesynthetiseerd

- Hoge efficiëntie, goedkope katalysator voor waterelektrolyse

- Herbevestigen van de waarde van internationale samenwerkingen

 De geboorte van een sneeuwpop aan de rand van het zonnestelsel
De geboorte van een sneeuwpop aan de rand van het zonnestelsel Kunstmatige huid zweet op commando
Kunstmatige huid zweet op commando Wat voor soort veranderingen zijn smelten en bevriezen?
Wat voor soort veranderingen zijn smelten en bevriezen?  Hoe lang duurt het voordat de mineralen in een rots worden gevormd?
Hoe lang duurt het voordat de mineralen in een rots worden gevormd?  Kan Mars van de aarde worden gezien?
Kan Mars van de aarde worden gezien?  Landvormen geproduceerd door de wind heten?
Landvormen geproduceerd door de wind heten?  Hoe is hydro -elektrisch vermogen slecht?
Hoe is hydro -elektrisch vermogen slecht?  Zijn deeltjes van een gas dicht bij elkaar?
Zijn deeltjes van een gas dicht bij elkaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

